第一节 弱电解质的电离(导学案)学习目标:强、弱电解质的概念和弱电解质的电离平衡相关知识链接---化学平衡 旧知回顾:电解质与非电解质【实验】先测反应前溶液的 pH 值,再进行与镁条的反应
一、强弱电解质:1
强电解质概念 2
弱电解质概念 二、电离平衡1
电离平衡的建立小组探究一(1) 醋酸在电离过程中各微粒浓度的变化
c(H+)c(CH3COO -)c(CH3COOH)CH3COOH 初溶于水紧接着最后(2)开始时,V(电离) 和 V(结合)怎样变化
(3)当 V 电离 = V 结合时,可逆过程达到一种什么样的状态
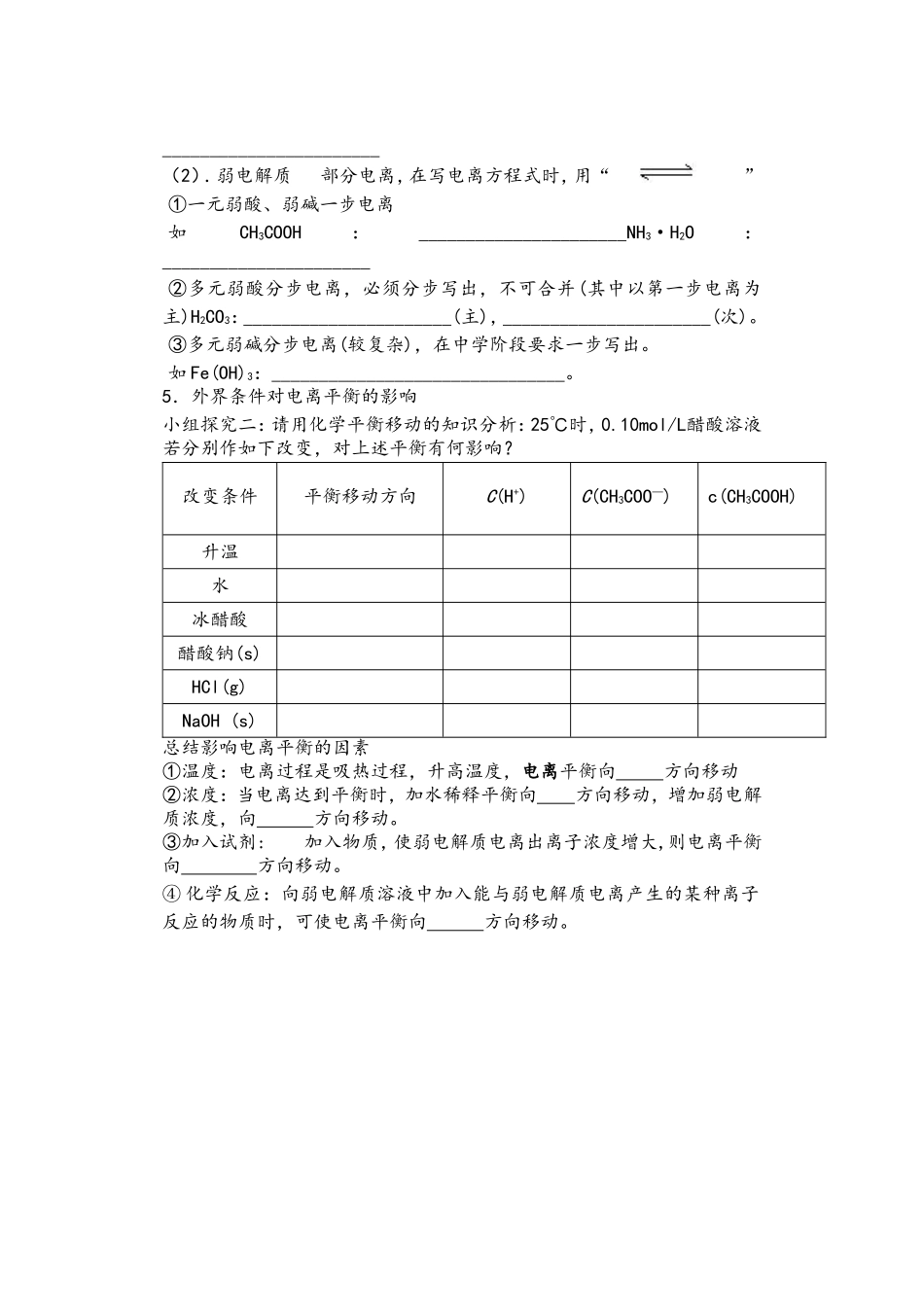
(4))弱电解质电离平衡状态建立示意图二、弱电解质的电离平衡2.定义 在一定条件(如温度、浓度)下,当电解质分子____的速率和_____的速率相等时,电离过程就达到了平衡状态.3.特征4、强弱电解质电离方程式的书写(小组互助完成)(1).强电解质 完全电离,在写电离方程式时,用“=”如H2SO4:________________________Ba(OH)2: 项 目1mol/L HCl1mol/L CH3COOH溶液 pH 的大小与足量镁条反应产生气泡的速度比较时间反应速率_______________________(2).弱电解质 部分电离,在写电离方程式时,用“ ”①一元弱酸、弱碱一步电离如CH3COOH:______________________NH3·H2O: ______________________②多元弱酸分步电离,必须分步写出,不可合并(其中以第一步电离为主)H2CO3:______________________(主),______________________(次)
③多元弱碱分步电离(较复杂),在中学阶段要求一步写出
如 Fe(OH)3:_______________________________
5.外界条件对电离平衡