第25 讲 常见气体的实验室制备、净化和收集 [复习目标] 1
了解常见气体的制备原理、装置及改进
能根据气体的性质及制备原理设计实验流程
1.气体制备实验的基本思路 2.重要气体的发生装置 依据制备气体所需的反应物状态和反应条件,可将制备气体的发生装置分为三类: (1)固体+固体――→△气体 制备气体:O2、NH3、CH4 等
(2)固体+液体(或液体+液体)――→△气体 制备气体:Cl2、C2H4 等
(3)固体+液体(不加热)―→气体 制备气体:选择合适的药品和装置能制取中学化学中常见的气体
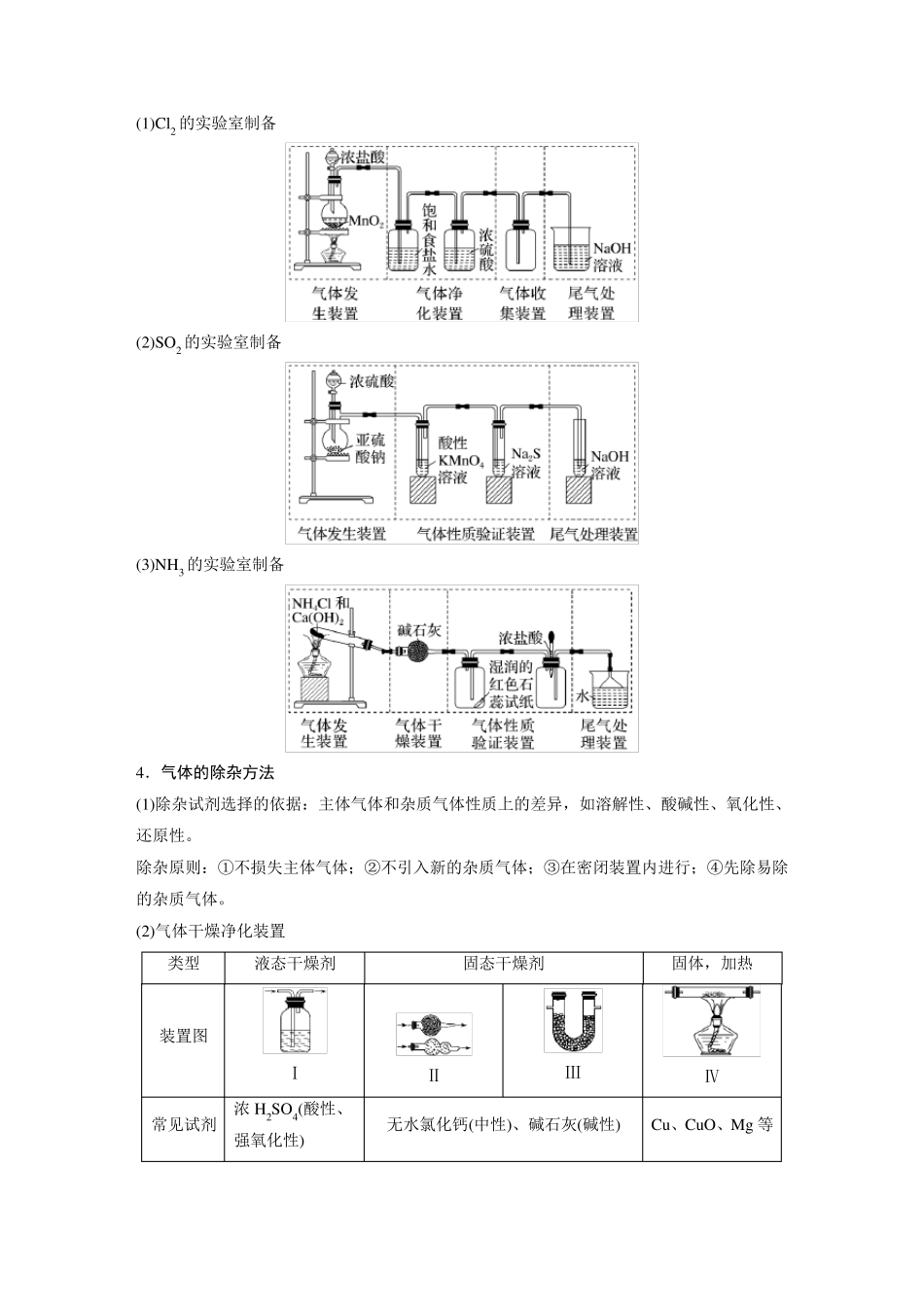
3.常见气体典型制备装置举例 (1)Cl2 的实验室制备 (2)SO2 的实验室制备 (3)NH3 的实验室制备 4.气体的除杂方法 (1)除杂试剂选择的依据:主体气体和杂质气体性质上的差异,如溶解性、酸碱性、氧化性、还原性
除杂原则:①不损失主体气体;②不引入新的杂质气体;③在密闭装置内进行;④先除易除的杂质气体
(2)气体干燥净化装置 类型 液态干燥剂 固态干燥剂 固体,加热 装置图 Ⅰ Ⅱ Ⅲ Ⅳ 常见试剂 浓H2SO4(酸性、强氧化性) 无水氯化钙(中性)、碱石灰(碱性) Cu、CuO、Mg 等 当CO2 中混有O2 杂质时,应选用上述Ⅰ~Ⅳ中的Ⅳ装置除O2,除杂试剂是Cu 粉
5.气体的收集方法 收集方法 收集气体的类型 收集装置 可收集的气体(举例) 排水法 难溶于水或微溶于水,且不与水反应的气体 O2、H2、NO、CO 等 排空气法 向上排空气法 密度大于空气且不与空气中的成分反应 Cl2、SO2、NO2、CO2 向下排空气法 密度小于空气且不与空气中的成分反应 H2、NH3 6
集气装置的创新——排液集气装置 (1)装置(Ⅰ)从a 管进气b 管出水可收集难溶于水的气体,如H2、O2 等
若将广口瓶中的液体更换,还可以收集以下气体
①饱和食盐水—