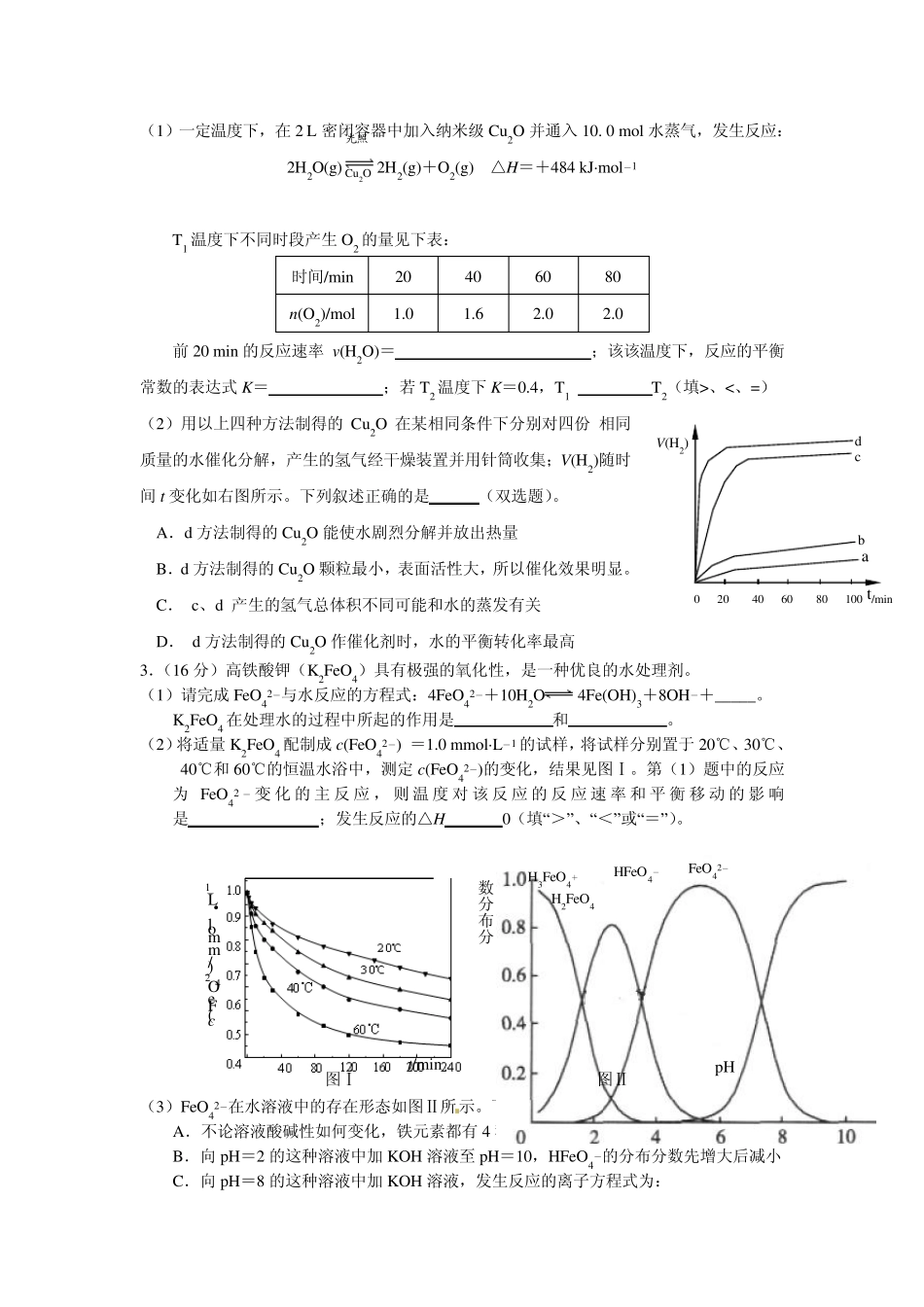
化学反应原理大题练习 1.(16 分)苯乙烯(C6H5CH=CH2)是生产各种塑料的重要单体,其制备原理是: C6H5C2H5(g)C6H5CH=CH2(g)+H2 (g) △H=+125kJ·mol-1 (1)该反应的平衡常数表达式为 K= __ _____________
随着温度的升高,K 值________(填“增大”、“减小”或“不变”,下同)
(2)实际生产中常以高温水蒸气作为反应体系的稀释剂(稀释剂不参加反应)
C6H5C2H5的平衡转化率与水蒸气的用量、体系总压强关系如下图
①由上图可得出: 结论一:其他条件不变,水蒸气的用量越大,平衡转化率越______; 结论二:__________________________________________________
②加入稀释剂能影响 C6H5C2H5 平衡转化率的原因是:_______________________
(3)某些工艺中,在反应的中途加入 O2 和特定的催化剂,有利于提高 C6H5C2H5 的平衡转化率
试解释其原因:_______________________________________________
2.(16 分)科学研究发现纳米级的 Cu2O 可作为太阳光分解水的催化剂
Ⅰ.四种制取Cu2O 的方法 (a)用炭粉在高温条件下还原 CuO 制备 Cu2O; (b)用葡萄糖还原 悬浊液制备 Cu2O; (c)电解法制备 Cu2O
原理如右图所示,反应为:2Cu+H2O=Cu2O+H2↑,则铜作为 极; (d)最新实验研究加热条件下用液态肼(N2H4)还原新制 Cu(OH)2 可制备纳米级Cu2O,同时放出 N2 和水蒸气
该制法的化学方程式为
Ⅱ.用制得的Cu2O 进行催化分解水的实验 平衡转化率/% 101kPa(900K) 40 60 80 4 8 12