关于物质的量的计算1、物质的量的基本概念(1)物质的量:表示含一定数目粒子的集合体
符号:n(2)摩尔:物质的量的单位
符号:mol(3)摩尔质量:单位物质的量的物质所具有的质量
符号:M单位:g/mol(4)阿伏加德罗常数:12g12C所含碳原子的个数
符号:NA,单位:mol-1(5)气体摩尔体积:单位物质的量的气体所占的体积
符号:Vm单位:L·mol-1(6)物质的量浓度:单位体积溶液里所含溶质的物质的量
符号:c单位mol·L-1(7)阿伏加德罗定律:同温同压下,相同体积的任何气体含有相同数目的粒子三个概念间的关系:物质的量(n)-摩尔(mol)-NA(物理量)(单位)(标准)2
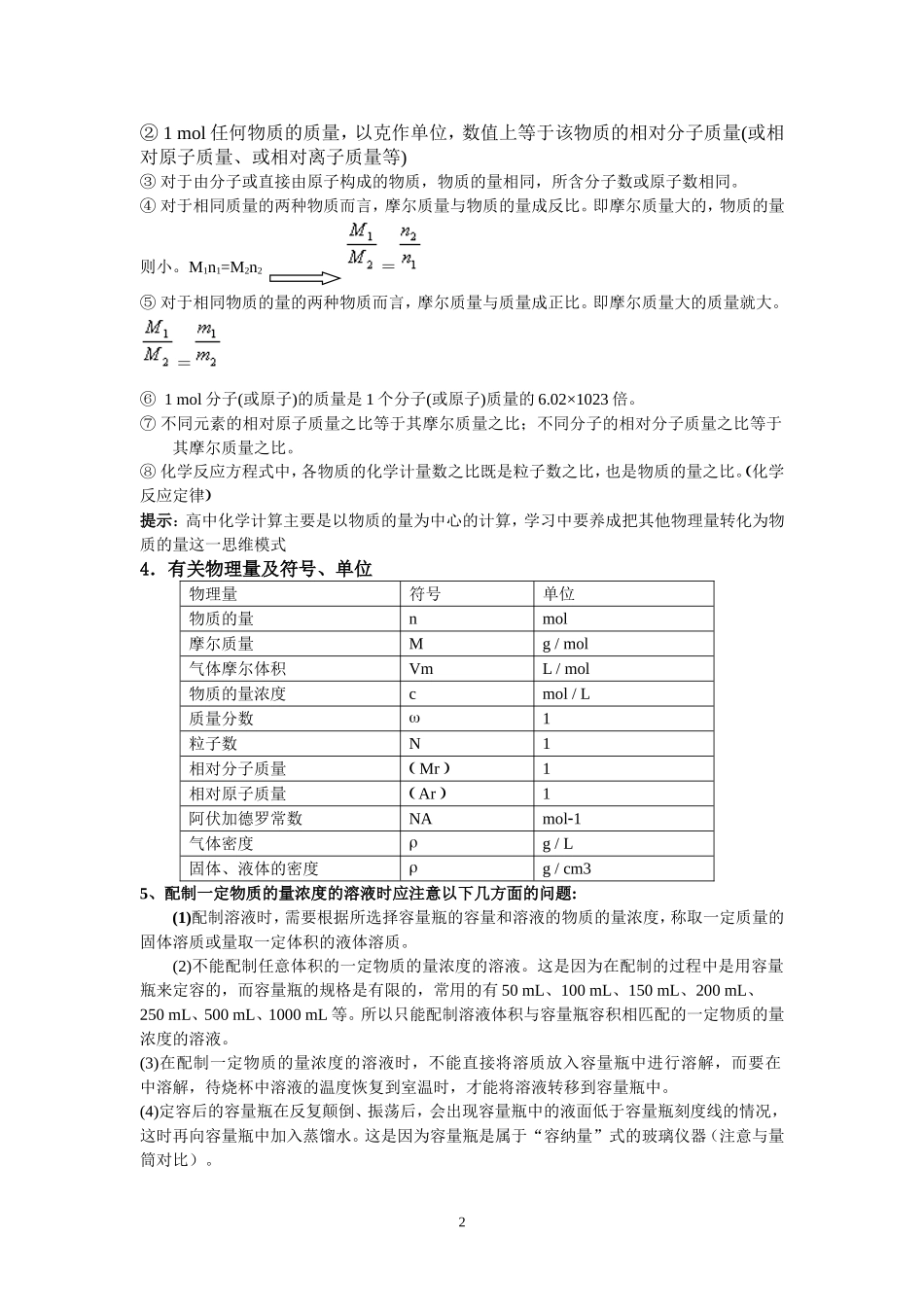
有关以物质的量为中心的计算:(1)n=(m/M)=(V/Vm)=(N/NA)=(c×V)(2)有关物理量之间的相互关系建立物质的量的好处在于:①它反映了化学反应的实质;②它把看不见的、不可量度的粒子数(微观量)和看得见的、可量度的质量或体积(宏观量)联系起来了;③它把气体的体积和分子数联系起来了;④可以建立以物质的量为中心的,联系其它各种物理量的一个完整的化学计算体系;⑤由于化学方程式中各物质的化学计量数之比既是粒子数比,又是物质的量之比,也是相同条件下气体的体积比
这种比值较相应的质量比简单,因此,用物质的量的关系进行计算就比较简捷
3.有关物质的量的八关系:①1mol任何物质都含有阿伏加德罗常数个粒子,即近似为6
02×1023个粒子
1②1mol任何物质的质量,以克作单位,数值上等于该物质的相对分子质量(或相对原子质量、或相对离子质量等)③对于由分子或直接由原子构成的物质,物质的量相同,所含分子数或原子数相同
④对于相同质量的两种物质而言,摩尔质量与物质的量成反比
即摩尔质量大的,物质的量则小
M1n1=M2n2=⑤对于相同物质的量的两种物质而言,摩尔质量与质量成正比
即摩尔质量大