3金属性结合;§2
4范德瓦耳斯结合;§2
5元素和化合物晶体结合的规律性1
教学目的和要求:通过讲解使学生理解并掌握金属性结合和范德瓦耳斯结合;理解元素和化合物晶体结合的规律性2.教学重点:金属性结合和范德瓦耳斯结合
3.教学难点:范德瓦耳斯结合
4.讲授时间:45分钟
5.讲授方式:PPT文档
6.作业:学生课后复习
一.金属性结合(1)金属性结合的概念第I族、第II族元素及过渡元素都是典型的金属晶体,它们的最外层电子一般为1~2个
组成晶体时每个原子的最外层电子为所有原子所共有,因此在结合成金属晶体时,失去了最外层(价)电子的原子实“沉浸”在由价电子组成的“电子云”中
如图XCH002_004所示
这种情况下,电子云和原子实之间存在库仑作用,体积越小电子云密度越高,库仑相互作用的能愈低,表现为原子聚合起来的作用
(2)金属晶体结合力金属晶体结合力:主要是原子实和电子云之间的静电库仑力,对晶体结构没有特殊的要求,只要求排列最紧密,这样势能最低,结合最稳定
因此大多数金属具有面心立方结构,即立方密积或六角密积,配位数均为12
立方密积(Cu、Ag、Au、Al)(面心立方结构)(配位数12)六角密积(Be、Mg、Zn、Cd)体心立方结构(Li、Na、K、Rb、Cs、Mo、W)(配位数8)良好的导电本领,结合能比前面两种晶体要低一些,过渡金属的结合能较大
晶体的平衡是依靠库仑作用力和一定的排斥力而维持的
排斥来自两个方面(a)但体积减小,电子云的密度增大,电子的动能将增加(b)当原子实相互接近到一定的距离时,它们的电子云发生显著的重叠,将产生强烈的排斥作用
金属性结合对原子的排列没有特殊的要求,这使得容易造成原子排列的不规范性,使其具有很大的范性
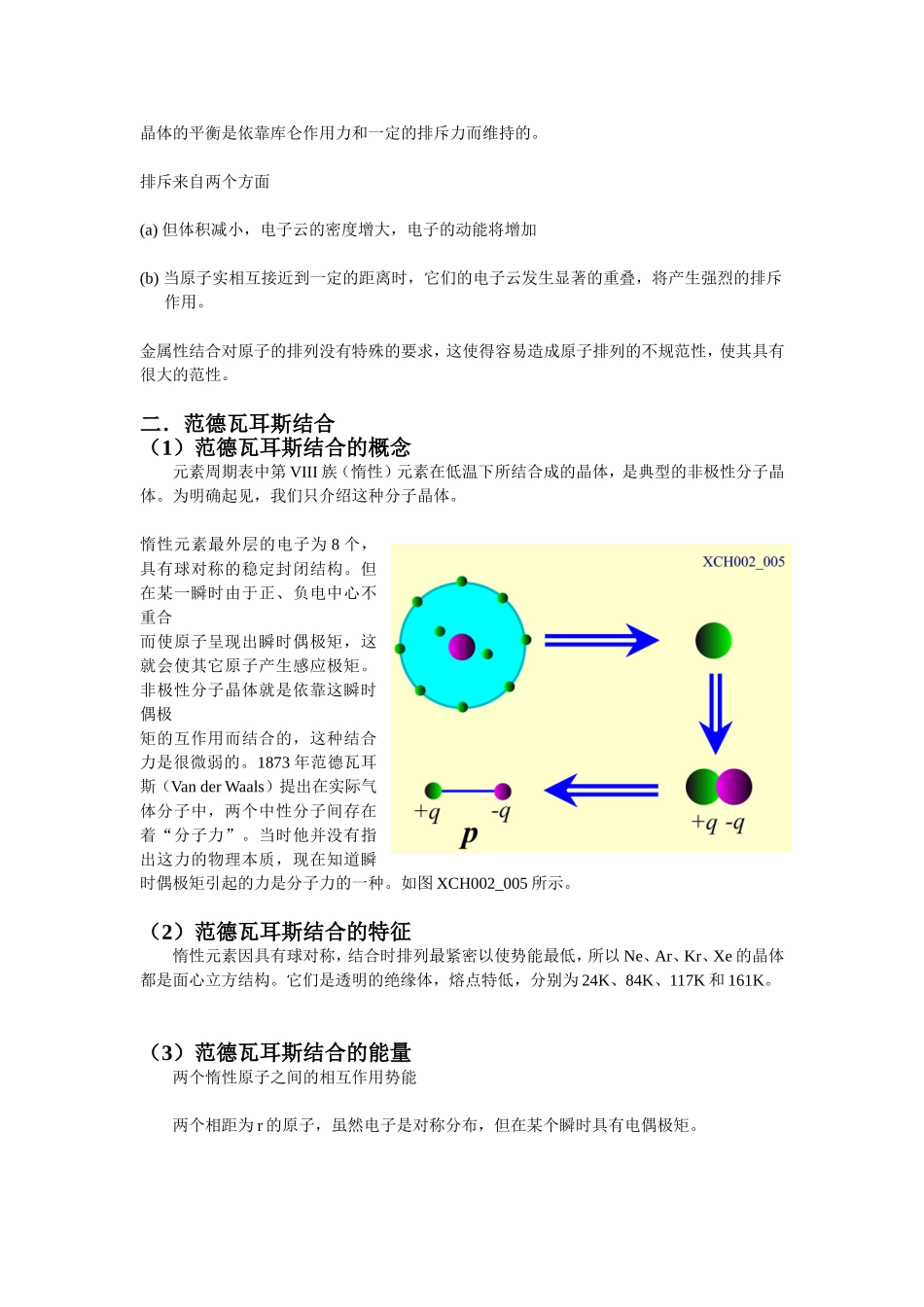
二.范德瓦耳斯结合(1)范德瓦耳斯结合的概念元素周期表中第VIII族(惰性)元素在低温下所结合成的晶体,是典型的非极性分子晶