1 电池电动势测定与热力学函数测定 姓名陈博殷 学号 20112401073 年级 11化 4 课程名称 物理化学实验 实验时间 2014/3/19 指导老师 蔡跃鹏、林晓明 一、【实验目的】 1、掌握电位差计的测量原理和测量电池电动势的方法; 2、加深对可逆电池,可逆电极、盐桥等概念的理解; 3、测定电池(1)的电动势; 4、掌握电动势法测定化学反应热力学函数变化值的有关原理和方法; 5、根据可逆热力学体系的要求设计可逆电池,测定其在不同温度下的电动势值,计算电池反应的热力学函数△G、△S、△H
二、【实验原理】 1、用对消法测定原电池电动势: 原因:原电池电动势不能用伏特计直接测量,因为电池与伏特计连接后有电流通过,就会在电极上发生生极化,结果使电极偏离平衡状态
另外,电池本身有内阻,所以伏特计测得的只是不可逆电池的端电压
而测量可逆电池的电动势,只能在无电流通过电池的情况下进行,因此,采用对消法
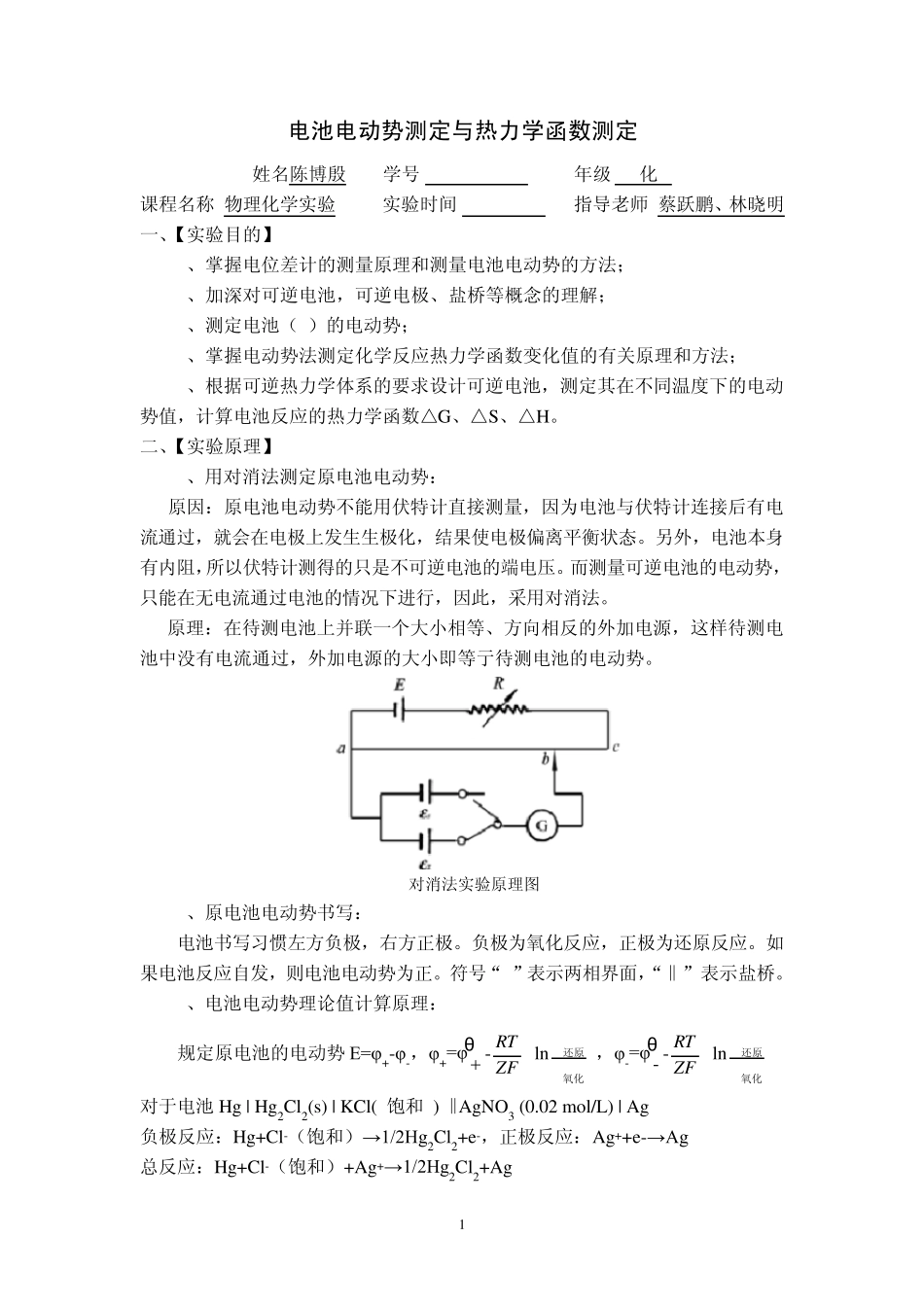
原理:在待测电池上并联一个大小相等、方向相反的外加电源,这样待测电池中没有电流通过,外加电源的大小即等亍待测电池的电动势
对消法实验原理图 2、原电池电动势书写: 电池书写习惯左方负极,右方正极
负极为氧化反应,正极为还原反应
如果电池反应自发,则电池电动势为正
符号“|”表示两相界面,“‖”表示盐桥
3、电池电动势理论值计算原理: 规定原电池的电动势 E=φ+-φ-,φ+=φθ - ZFRT ln氧化还原αα ,φ-=φθ- - ZFRT ln氧化还原αα 对于电池 Hg | Hg2Cl2(s) | KCl( 饱和 ) ‖AgNO3 (0
02 mol/L) | Ag 负极反应:Hg+Cl-(饱和)→ 1/2Hg2Cl2+e-,正极反应:Ag++e-→ Ag 总反应:Hg+Cl-(饱和)+Ag+→ 1/2Hg2Cl2+Ag 2 正极银电极的电极电位:φAg/Ag+