课时梯级作业十七化学能与热能(45分钟100分)一、选择题(本题包括9小题,每题6分,共54分)1
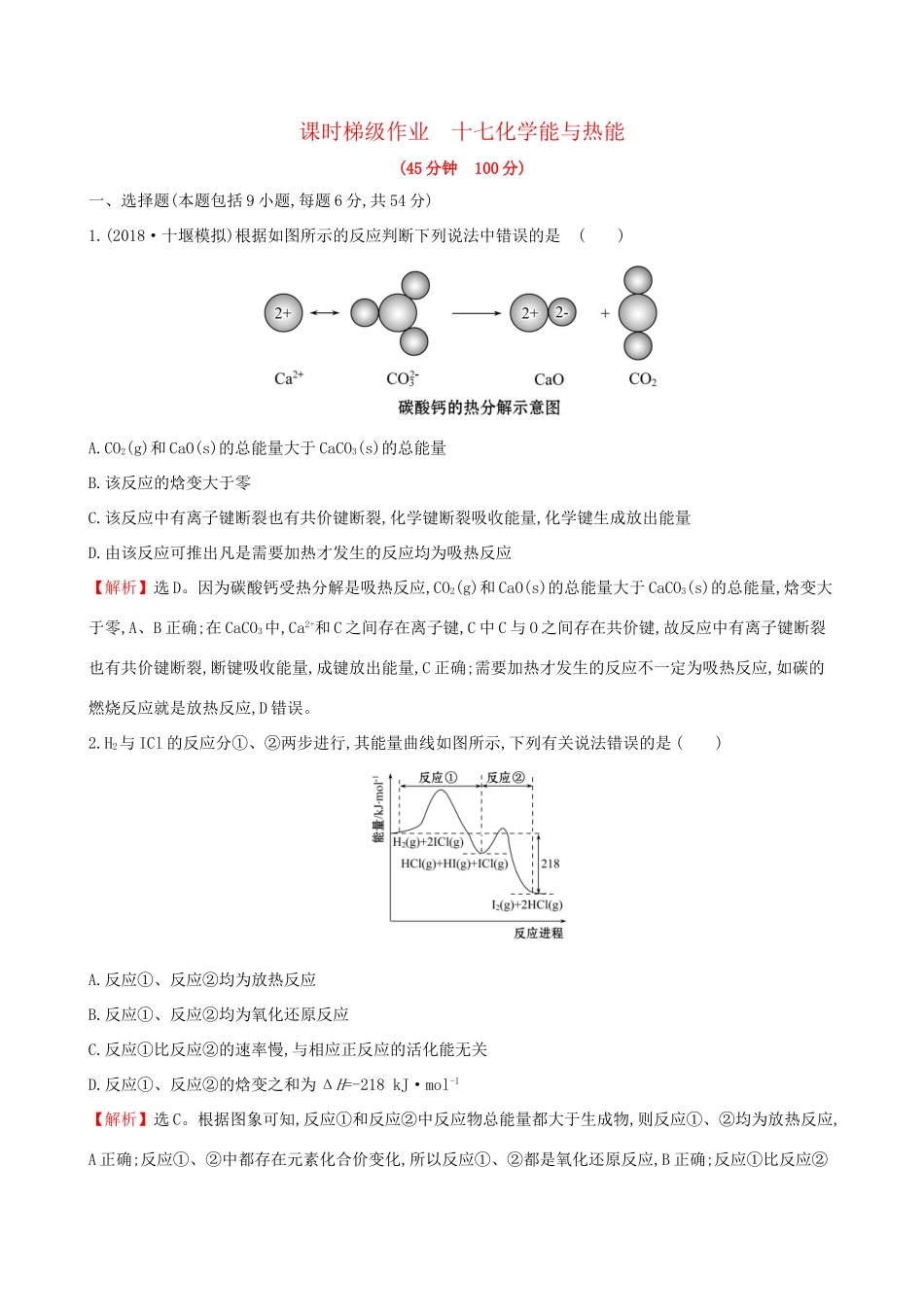
(2018·十堰模拟)根据如图所示的反应判断下列说法中错误的是()A
CO2(g)和CaO(s)的总能量大于CaCO3(s)的总能量B
该反应的焓变大于零C
该反应中有离子键断裂也有共价键断裂,化学键断裂吸收能量,化学键生成放出能量D
由该反应可推出凡是需要加热才发生的反应均为吸热反应【解析】选D
因为碳酸钙受热分解是吸热反应,CO2(g)和CaO(s)的总能量大于CaCO3(s)的总能量,焓变大于零,A、B正确;在CaCO3中,Ca2+和C之间存在离子键,C中C与O之间存在共价键,故反应中有离子键断裂也有共价键断裂,断键吸收能量,成键放出能量,C正确;需要加热才发生的反应不一定为吸热反应,如碳的燃烧反应就是放热反应,D错误
H2与ICl的反应分①、②两步进行,其能量曲线如图所示,下列有关说法错误的是()A
反应①、反应②均为放热反应B
反应①、反应②均为氧化还原反应C
反应①比反应②的速率慢,与相应正反应的活化能无关D
反应①、反应②的焓变之和为ΔH=-218kJ·mol-1【解析】选C
根据图象可知,反应①和反应②中反应物总能量都大于生成物,则反应①、②均为放热反应,A正确;反应①、②中都存在元素化合价变化,所以反应①、②都是氧化还原反应,B正确;反应①比反应②的速率慢,说明反应①中正反应的活化能较大,反应②中正反应的活化能较小,C错误;反应①、反应②总的能量变化为218kJ,根据盖斯定律可知,反应①、反应②的焓变之和为ΔH=-218kJ·mol-1,D正确
(2018·盐城模拟)利用CO2和CH4重整可制合成气(主要成分为CO、H2)
下列有关说法正确的是()①CH4(g)C(s)+2H2(g)ΔH1=+75
0kJ·mol-1②CO2(g)+H2(g)CO(g