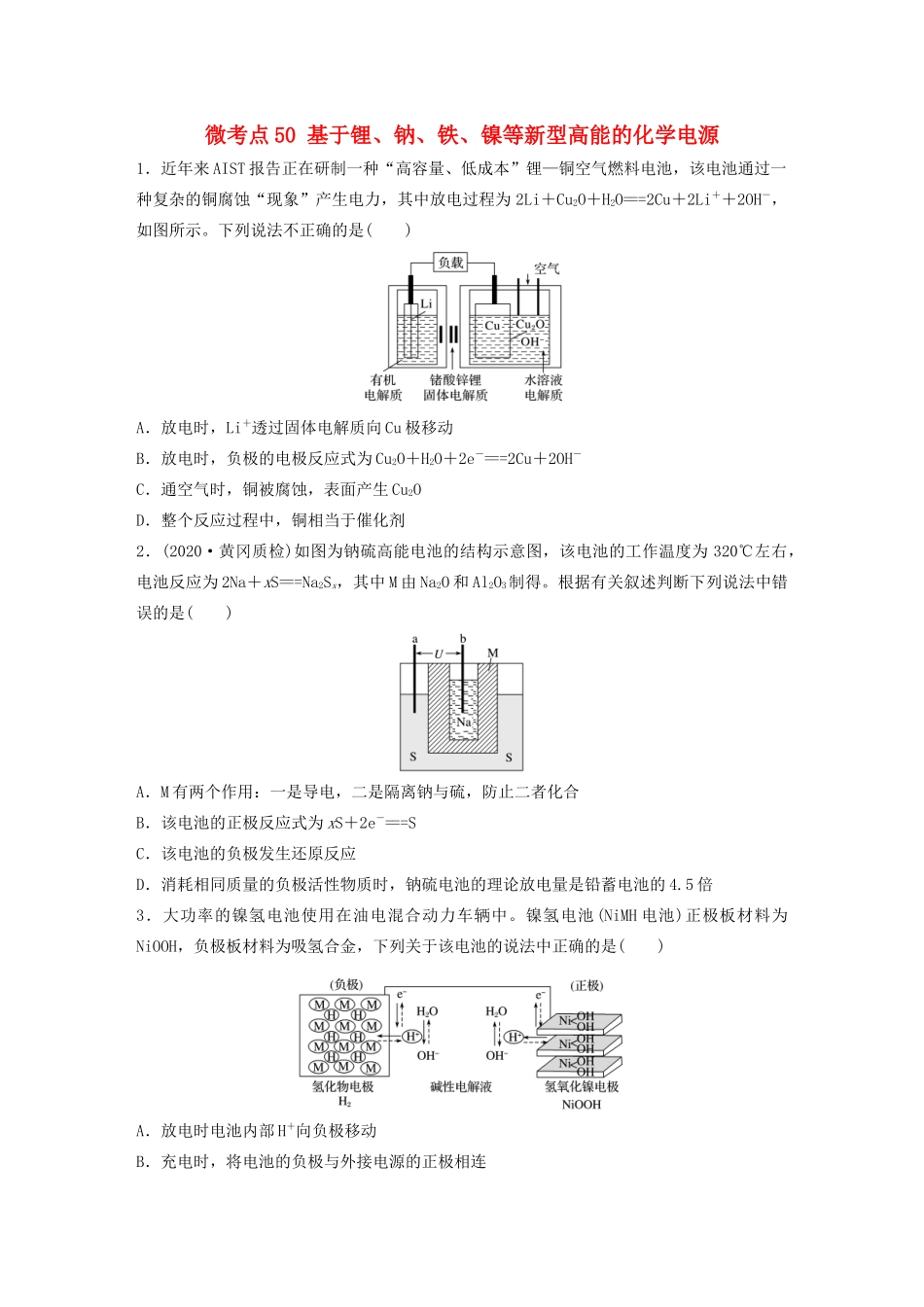
微考点50基于锂、钠、铁、镍等新型高能的化学电源1.近年来AIST报告正在研制一种“高容量、低成本”锂—铜空气燃料电池,该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O===2Cu+2Li++2OH-,如图所示
下列说法不正确的是()A.放电时,Li+透过固体电解质向Cu极移动B.放电时,负极的电极反应式为Cu2O+H2O+2e-===2Cu+2OH-C.通空气时,铜被腐蚀,表面产生Cu2OD.整个反应过程中,铜相当于催化剂2.(2020·黄冈质检)如图为钠硫高能电池的结构示意图,该电池的工作温度为320℃左右,电池反应为2Na+xS===Na2Sx,其中M由Na2O和Al2O3制得
根据有关叙述判断下列说法中错误的是()A.M有两个作用:一是导电,二是隔离钠与硫,防止二者化合B.该电池的正极反应式为xS+2e-===SC.该电池的负极发生还原反应D.消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的4
5倍3.大功率的镍氢电池使用在油电混合动力车辆中
镍氢电池(NiMH电池)正极板材料为NiOOH,负极板材料为吸氢合金,下列关于该电池的说法中正确的是()A.放电时电池内部H+向负极移动B.充电时,将电池的负极与外接电源的正极相连C.充电时阳极反应式为Ni(OH)2+OH--e-===NiOOH+H2OD.放电时负极的电极反应式为MHn-ne-===M+nH+4.高铁电池是一种新型可充电电池,电解质溶液为KOH溶液,充放电时的总反应式为3Zn+2K2FeO4+8H2O3Zn(OH)2+2Fe(OH)3+4KOH
下列叙述正确的是()A.放电时,负极反应式为3Zn-6e-+6OH-===3Zn(OH)2B.放电时,正极区溶液的pH减小C.充电时,每转移3mol电子,阳极有1molFe(OH)3被还原D.充电时,电池的锌电极接电源的