第四单元 金属元素及其化合物能力提升金属及其化合物的转化1
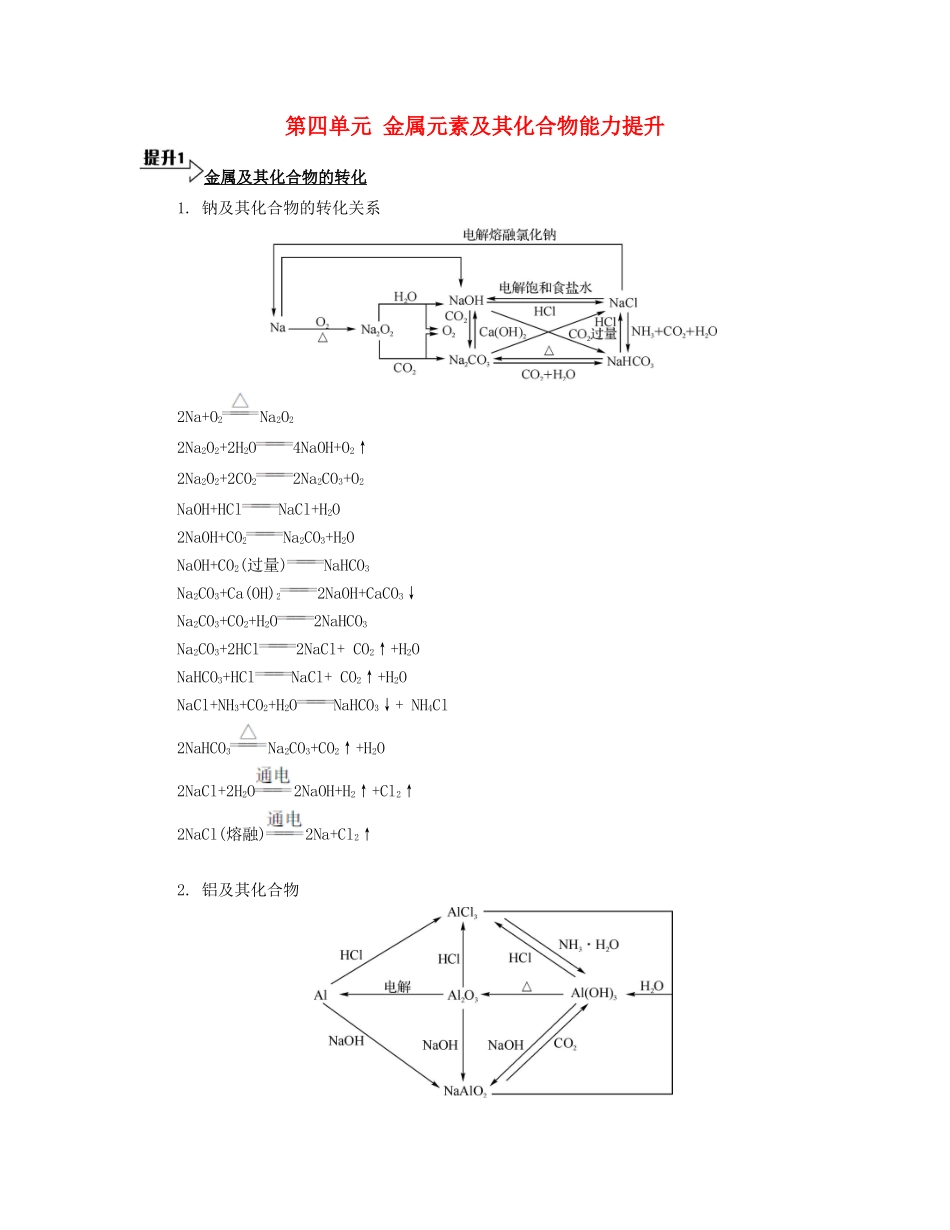
钠及其化合物的转化关系2Na+O2Na2O22Na2O2+2H2O4NaOH+O2↑2Na2O2+2CO22Na2CO3+O2NaOH+HClNaCl+H2O2NaOH+CO2Na2CO3+H2ONaOH+CO2(过量)NaHCO3Na2CO3+Ca(OH)22NaOH+CaCO3↓Na2CO3+CO2+H2O2NaHCO3Na2CO3+2HCl2NaCl+ CO2↑+H2ONaHCO3+HClNaCl+ CO2↑+H2ONaCl+NH3+CO2+H2ONaHCO3↓+ NH4Cl2NaHCO3Na2CO3+CO2↑+H2O2NaCl+2H2O2NaOH+H2↑+Cl2↑2NaCl(熔融)2Na+Cl2↑2
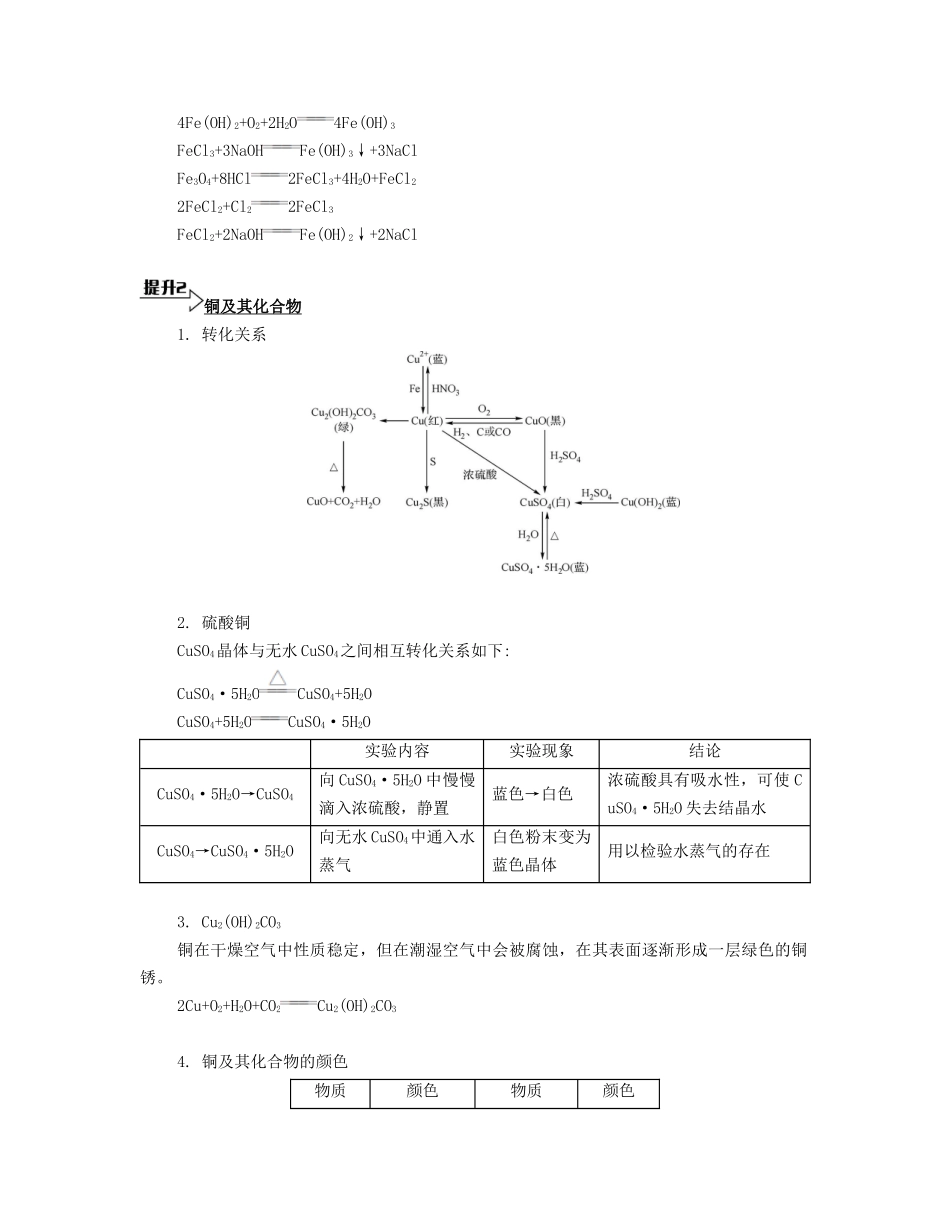
铝及其化合物2Al+6HCl2AlCl3+3H2↑2Al+2NaOH+2H2O2NaAlO2+3H2↑Al2O3+6HCl2AlCl3+3H2O2Al(OH)3Al2O3+3H2O2Al2O3(熔融)4Al+3O2↑Al2O3+2NaOH2NaAlO2+H2OAl(OH)3+NaOHNaAlO2+2H2O2NaAlO2+CO2+3H2O2Al(OH)3↓+Na2CO3NaAlO2+CO2(过量)+2H2OAl(OH)3↓+NaHCO3Al(OH)3+3HClAlCl3+3H2OAlCl3+3NH3·H2OAl(OH)3↓+3NH4Cl AlCl3+3NaAlO2+6H2O4Al(OH)3↓+3NaCl3
铁及其化合物3Fe+2O2Fe3O43Fe+4H2O(g)Fe3O4+4H2↑2Fe+3Cl22FeCl38Al+3Fe3O44Al2O3+9Fe2Al+Fe2O3Al2O3+2Fe3CO+Fe2O33CO2+2FeFe+2HClFeCl2+ H2↑FeO+2HClFeCl2+H2O2FeCl3+Fe3F