专题三 化学工艺流程题型研究能力展示1
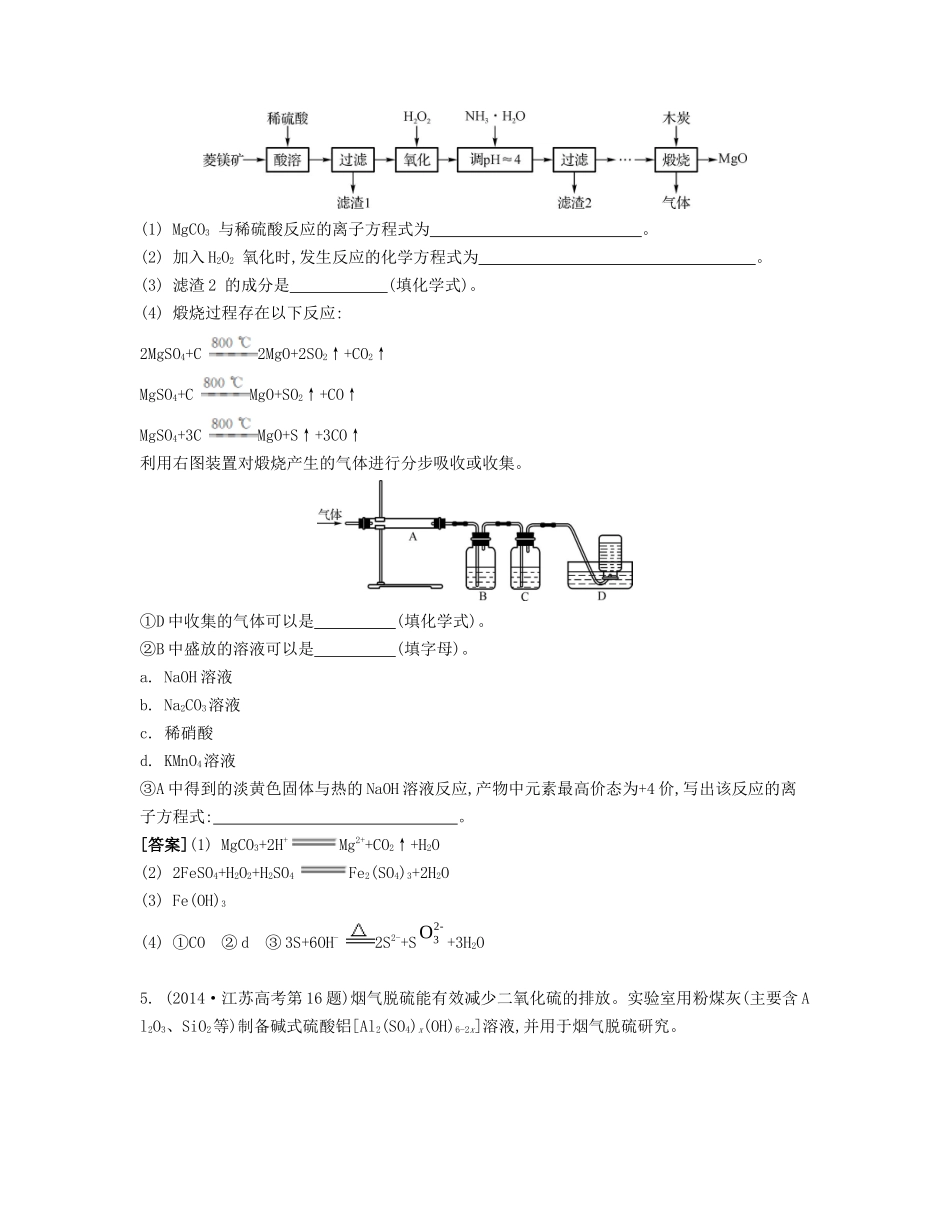
(2010·江苏高考第 16 题)钡盐行业生产中排出大量的钡泥[主要含有 BaCO3、BaSiO3、BaSO3、Ba(FeO2)2等]
某主要生产 BaCl2、BaCO3、BaSO4的化工厂利用钡泥制取 Ba(NO3)2,其部分工艺流程如下:(1) 酸溶后溶液中 pH=1,Ba(FeO2)2与 HNO3反应的化学方程式为
(2) 酸溶时通常控制反应温度不超过 70℃且不使用浓硝酸,原因是
(3) 该厂结合本厂实际,选用的 X 为 (填化学式);中和Ⅰ使溶液中 (填离子符号)的浓度减小(中和Ⅰ引起的溶液体积变化可忽略)
(4) 上述流程中洗涤的目的是
[答案](1) Ba(FeO2)2+8HNO3 Ba(NO3)2+2Fe(NO3)3+4H2O(2) 防止反应速度过快;浓硝酸易挥发、易分解(3) BaCO3 Fe3+、H+(4) 减少废渣中可溶性钡盐对环境的污染[解析](1) Ba(FeO2)2与 HNO3反应,生成对应的硝酸盐
(2) 控制温度,不用浓硝酸的目的是控制反应速率,防止反应速率过快;同时防止浓硝酸挥发、分解
(3) 通过产物,结合溶液的酸碱性,选用的 X 为 BaCO3,在Ⅰ中有 Fe3+、H+、Ba2+和 N等,加入 BaCO3后,能使 Fe3+和 H+浓度降低
(4) 在废渣中有可溶性钡盐,有毒,因此,洗涤的目的是减少可溶性钡盐对环境的污染
(2011·江苏高考第 16 题)以硫铁矿(主要成分为 FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:回答下列问题:(1) 一定条件下,SO2转化为 SO3的反应为 2SO2(g)+O2(g)2SO3(g),该反应的平衡常数表达-3O式为 K= ;过量的 SO2与 NaOH 溶液反应的化学方程式为
(2) 酸溶及后续过程中均需保持盐酸过量,其目