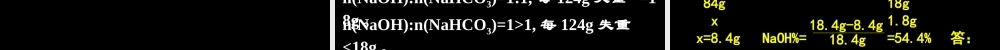过量计算过量计算方程式的计算方程式的计算有关化学有关化学 阅读课本阅读课本 P21-23P21-23
掌握:过量计算题型的基本特征:基本解题步骤:两种两种反应物的量都已知
1 、写出反应方程式2A+3B = C+2D2 、设估计过量的反应物与另一反应物完全反应所需量为X解:设与 amolA 完全反应的 B 的物质的量为 x3 、根据方程式列比例式求X 2 3amol xx=1
5a mol4 、比较 B 的已知量与x 的值,判断判断过量
5 、由不足量不足量的反应物的量进行计算
练习 1 :用消石灰和硫酸铵各 10g 混合加热, 将制得的氨气溶于水制成 200mL 氨水,求此氨水的物质的量浓度
解:设与 10g(NH4)2SO4 反应需 Ca(OH)2 的质量为X ,生成 NH3 的物质的量为n
(NH4)2SO4+Ca(OH)2=2NH3 +2H2O+CaSO4 132g 74g 2mol 10g x n x =5
6g1, 每 124g 失重