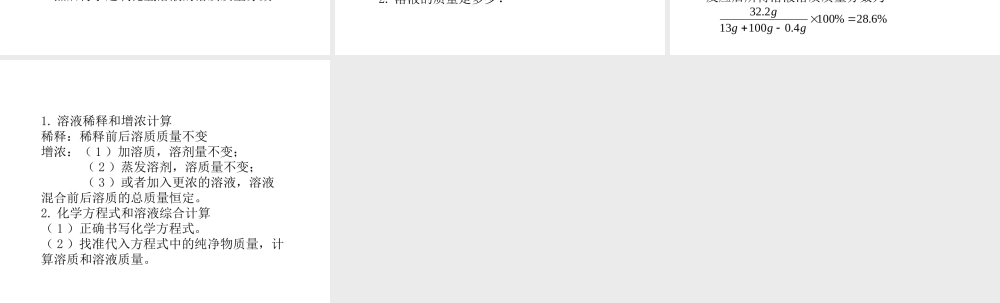
课题 3 溶液的浓度(第 2 课时) 许多化学反应都在溶液中进行,例如实验室用 5% 的过氧化氢溶液和二氧化锰制取氧气,而我们实验室里购买的过氧化氢溶液是 30% 的,为了在实验室达到反应速率适中的效果,我们需要将 30% 的过氧化氢溶液进行稀释。 问题情境引入一、稀释溶液设:需要水的质量为 x 。根据稀释前后溶质不变,得出如下关系:50g×30%=(50g+x) ×5%x=250g例:将 50g30% 的过氧化氢溶液稀释成5% 的过氧化氢溶液,需要水的质量是多少? 一、稀释溶液将 10g16% 的氯化钠溶液稀释成 4% 的溶液。1. 计算: 10g16% 的氯化钠溶液中溶质质量 g, 需要加水 ml 。2. 量取:选用 ml 量筒量取水。3. 混匀:将水倒入盛有 10g16% 的氯化钠溶液的烧杯中,用玻璃棒搅拌。4. 把稀释好的溶液倒入试剂瓶中,并贴上标签。1.63050二、化学反应与溶液计算 为测定某失去标签的过氧化氢溶液的溶质质量分数,现将 2.5g 二氧化锰放入盛有 100g 过氧化氢溶液的锥形瓶中,完全反应后,共收集到 1.6g 气体。过氧化氢溶液中溶质的质量分数是多少? 根据化学方程式计算,求出生成1.6g 氧气,参加反应的过氧化氢的质量,然后再求过氧化氢溶液的溶质质量分数。二、化学反应与溶液计算100 g 某硫酸溶液恰好与 13 g 锌完全起反应。试计算反应后所得溶液的溶质质量分数是多少?提示:1. 反应后得到溶液的溶质是什么?2. 溶液的质量是多少?设:生成硫酸锌的质量为 x ,生成氢气质量为 y 。Zn+H2SO4= ZnSO4+H2↑65 161 213g x y 65:98=13g:x x=32.2g65:98=13g:y y=0.4g硫酸中溶质质量分数为反应后所得溶液溶质质量分数为%6.19%1001006.19gg%6.28%1004.0100132.32gggg二、化学反应与溶液计算三、小结1. 溶液稀释和增浓计算稀释:稀释前后溶质质量不变增浓:( 1 )加溶质,溶剂量不变; ( 2 )蒸发溶剂,溶质量不变; ( 3 )或者加入更浓的溶液,溶液混合前后溶质的总质量恒定。 2. 化学方程式和溶液综合计算( 1 )正确书写化学方程式。( 2 )找准代入方程式中的纯净物质量,计算溶质和溶液质量。