第 6 讲 溶解度一、饱和溶液与不饱和溶液:在 下,在 里,不能再溶解某种溶质的溶液,叫 的饱和溶液
在一定温度下,在一定量的溶剂里,能继续溶解某种溶质的溶液,叫该溶质的不饱和溶液
一定温度一定量的溶剂该溶质对饱和溶液和不饱和溶液的理解:(1) 、要明确“一定温度”和“一定量溶剂”
因为改变溶剂量和温度时,饱和溶液与不饱和溶液可以相互转化的;(2) 、要明确“某一溶质”的饱和溶液或不饱和溶液
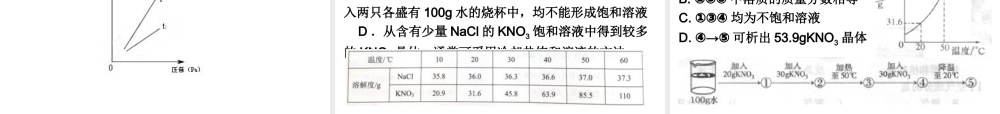
例:在一定温度下,不能再溶解 NaCl 的饱和溶液,可能还能溶解 KNO3
思考:下列说法有何不妥
对于同种溶质,饱和溶液一定比不饱和溶液的浓度大;2
相同温度下,对于同种溶质,饱和溶液一定比不饱和溶液含有的溶质多
1 、对于同种溶质的溶液来说,饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液;饱和溶液、不饱和溶液与浓稀溶液的关系2 、在同一温度下,同种溶质的饱和溶液一定比不饱和溶液浓度大
饱和溶液与不饱和溶液的转化条件一般规律:饱和溶液不饱和溶液升高溶液温度加入同种溶质加入溶剂降低溶液温度蒸发溶剂特殊情况:如氢氧化钙,温度越高,溶解 性越差
确定某种溶液是否饱和的方法⑴ 加入少量原溶质,若不能继续溶解,说明原溶液是该溶质的饱和溶液;⑵ 或者在一定温度下,看该溶液中有没有不能继续溶解的溶质存在,若有且溶质的量不再减少,说明原溶液是该溶质的饱和溶液
二、溶解度: 在 下,某固态物质在 g 溶剂(通常溶剂为水)里达到 时所溶解的质量
同一种固体在不同温度下的溶解度不同100g 是溶剂的质量,不是溶液的质量饱和状态单位: g一定温度饱和状态100溶解度的影响因素与溶质的种类、溶剂的种类和温度有关与溶质和溶剂的数量无关溶解度与溶解性0
01g1g10g难溶微溶可溶易溶三、溶解度曲线1 、溶解度曲线上的点表示: ;溶解度曲线下方的点表示: ;溶解度曲线上方的点表示:
2 、⑴大多数物质