2007级高一化学教学案勤奋创造奇迹,细节决定成败元素周期律(第二课时)教学目标:1、通过第三周期元素及化合物的性质变化掌握金属性、非金属的比较规律
2、了解元素周期律的反现对化学发展的意义
了解元素周期表的作用教学过程:一、元素周期律1、钠、镁、铝的金属性比较:⑴镁、铝分别与盐酸的反应:MgAl现象化学方程式⑵钠、镁、铝分别与水的反应:NaMgAl单质与水(或酸)反应与冷水:与冷水反应缓慢,与沸水反应迅速,放出氢气,与酸反应剧烈放出氢气与酸反应:最高价氧化物对应水化物的碱性强弱NaOH()Mg(OH)2中强碱Al(OH)3()结论:钠、镁、铝的金属性强弱的顺序是:
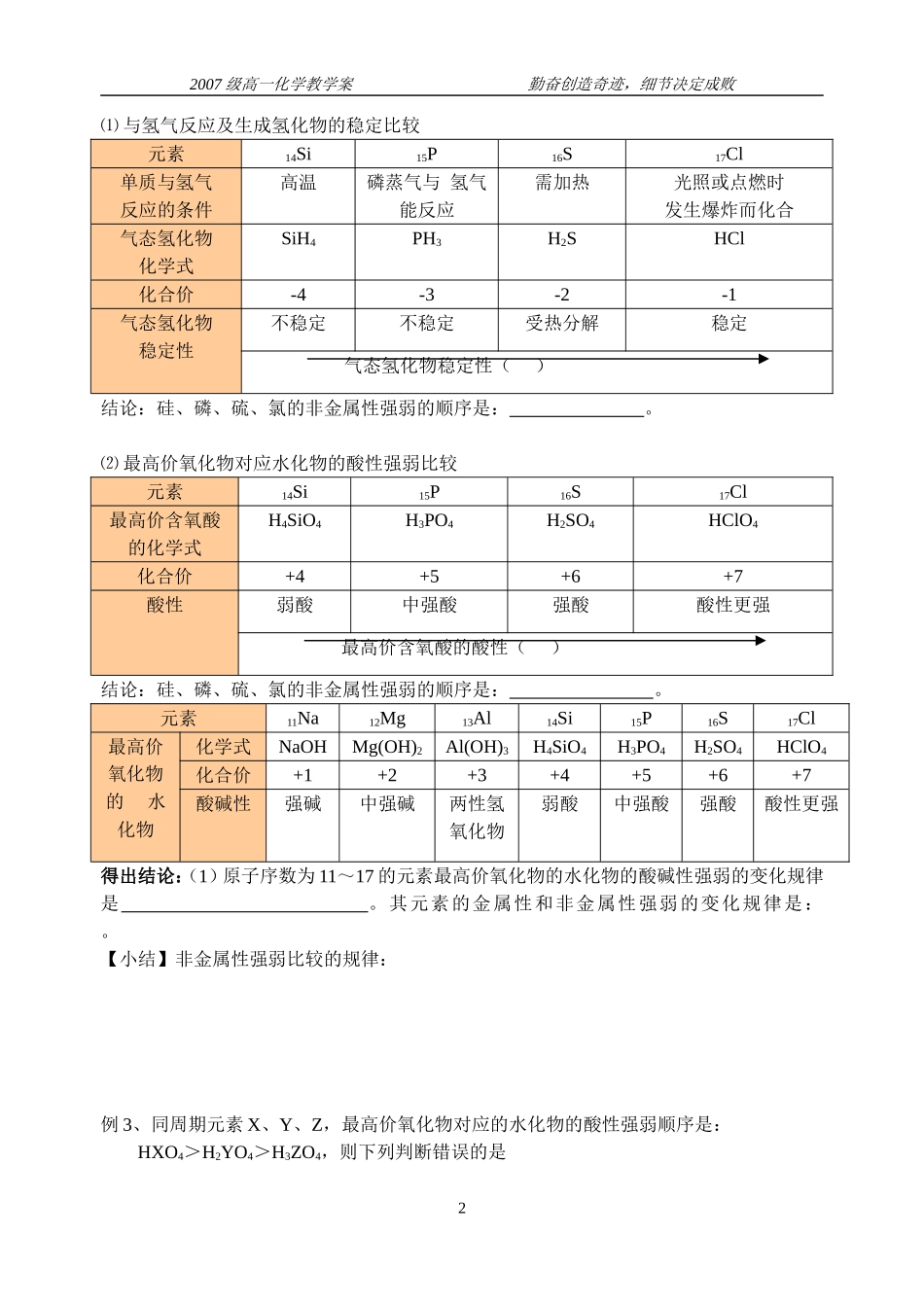
【小结】金属性强弱比较的规律:例1、能证明铝的金属性比镁弱的实验事实是A、铝的原子半径比镁小B、镁与浓硫酸反应,铝与冷的浓硫酸不反应C、Al(OH)3能溶于NaOH,而Mg(OH)2不能D、铝的金属光泽不如镁显著例2、下列叙述中能肯定A金属比B金属活泼性强的是A、A原子的最外层电子数比B原子的最外层电子数少B、常温下,A能从水中置换出氢,而B不能C、1molA从酸中置换出H+生成的H2比1molB从酸中置换出H+生成的H2多D、A原子的电子层数比B原子的电子层数多2、硅、磷、硫、氯的非金属性的比较:12007级高一化学教学案勤奋创造奇迹,细节决定成败⑴与氢气反应及生成氢化物的稳定比较元素14Si15P16S17Cl单质与氢气反应的条件高温磷蒸气与氢气能反应需加热光照或点燃时发生爆炸而化合气态氢化物化学式SiH4PH3H2SHCl化合价-4-3-2-1气态氢化物稳定性不稳定不稳定受热分解稳定气态氢化物稳定性()结论:硅、磷、硫、氯的非金属性强弱的顺序是:
⑵最高价氧化物对应水化物的酸性强弱比较元素14Si15P16S17Cl最高价含氧酸的化学式H4SiO4H3PO4H2SO4HClO4化合价+4+5+6+7酸性弱