2012级高一化学竞赛辅导材料[物质结构与性质]2012-12-20第三讲元素性质的递变规律一、学习目标:1、了解同一周期、同一主族中元素第一电离能的变化规律,了解元素电离能和原子核外电子排布的关系
2、了解同一周期、同一主族中元素电负性的变化规律,能根据元素的电负性说明周期表中元素金属性和非金属性的变化规律
二、教学内容:一、元素电离能第一电离能:气态电中性基态原子失去1个电子,转化为气态基态正离子所需要的能量叫做第一电离能
常用符号I1表示,单位为kJ/mol
原子核外电子排布的周期性
随着原子序数的增加,元素原子的外围电子排布呈现周期性的变化:每隔一定数目的元素,元素原子的外围电子排布重复出现从ns1到ns2np6的周期性变化
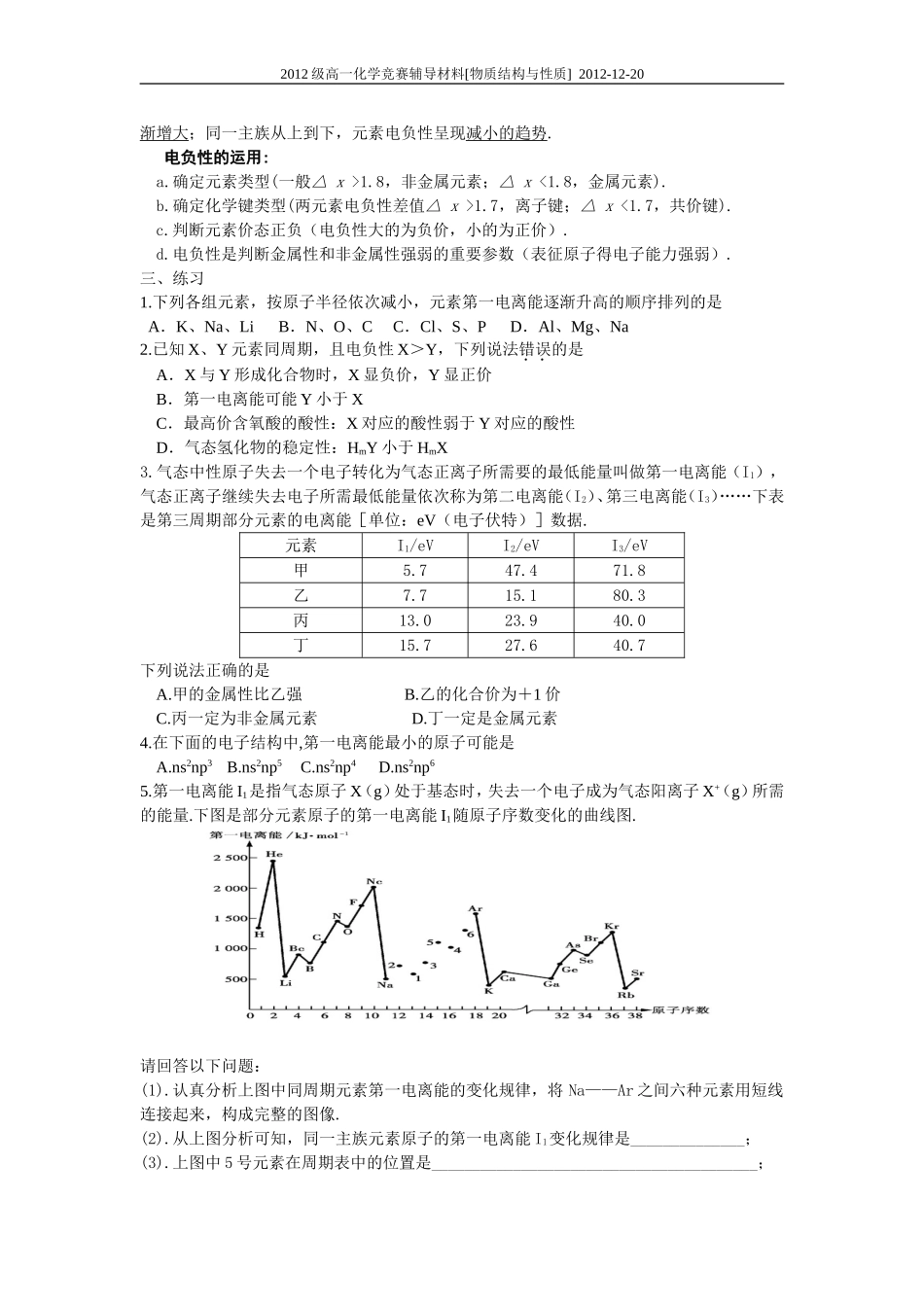
元素第一电离能的周期性变化
随着原子序数的递增,元素的第一电离能呈周期性变化:★同周期从左到右,第一电离能呈增大的趋势,稀有气体的第一电离能最大,碱金属的第一电离能最小;★同主族从上到下,第一电离能逐渐减小
说明:①同周期元素,从左往右第一电离能呈增大趋势
电子亚层结构为全满、半满时较相邻元素要大即第ⅡA族、第ⅤA族元素的第一电离能分别大于同周期相邻元素
Be、N、Mg、P②
元素第一电离能的运用:a
电离能是原子核外电子分层排布的实验验证
用来比较元素的金属性的强弱
I1越小,金属性越强,表征原子失电子能力强弱
元素电负性的周期性变化
元素的电负性(用X表示):元素的原子在分子中吸引电子对的能力叫做该元素的电负性
随着原子序数的递增,元素的电负性呈周期性变化:同周期从左到右,主族元素电负性逐2012级高一化学竞赛辅导材料[物质结构与性质]2012-12-20渐增大;同一主族从上到下,元素电负性呈现减小的趋势
电负性的运用:a
确定元素类型(一般△x>1
8,非金属元素;△x1
7,离子键;△x