第2课时化学反应与电能课程标准核心素养1
以原电池为例认识化学能可以转化为电能
从氧化还原反应的角度初步认识原电池的工作原理
能列举化学能转化为电能的实例,能辨识简单原电池的构成要素
宏观辨识与微观探析:能从宏观(能量变化)和微观(电子转移)相结合的视角分析原电池的组成和工作原理
科学探究与创新意识:能从有关原电池的问题和假设出发,依据探究目的,设计探究方案,运用化学实验进行实验探究
化学能转化为电能一、火力发电——化学能间接转化为电能1.能量转化过程化学能――→热能――→机械能――→电能2.化学能转化为电能的关键:燃烧(氧化还原反应)
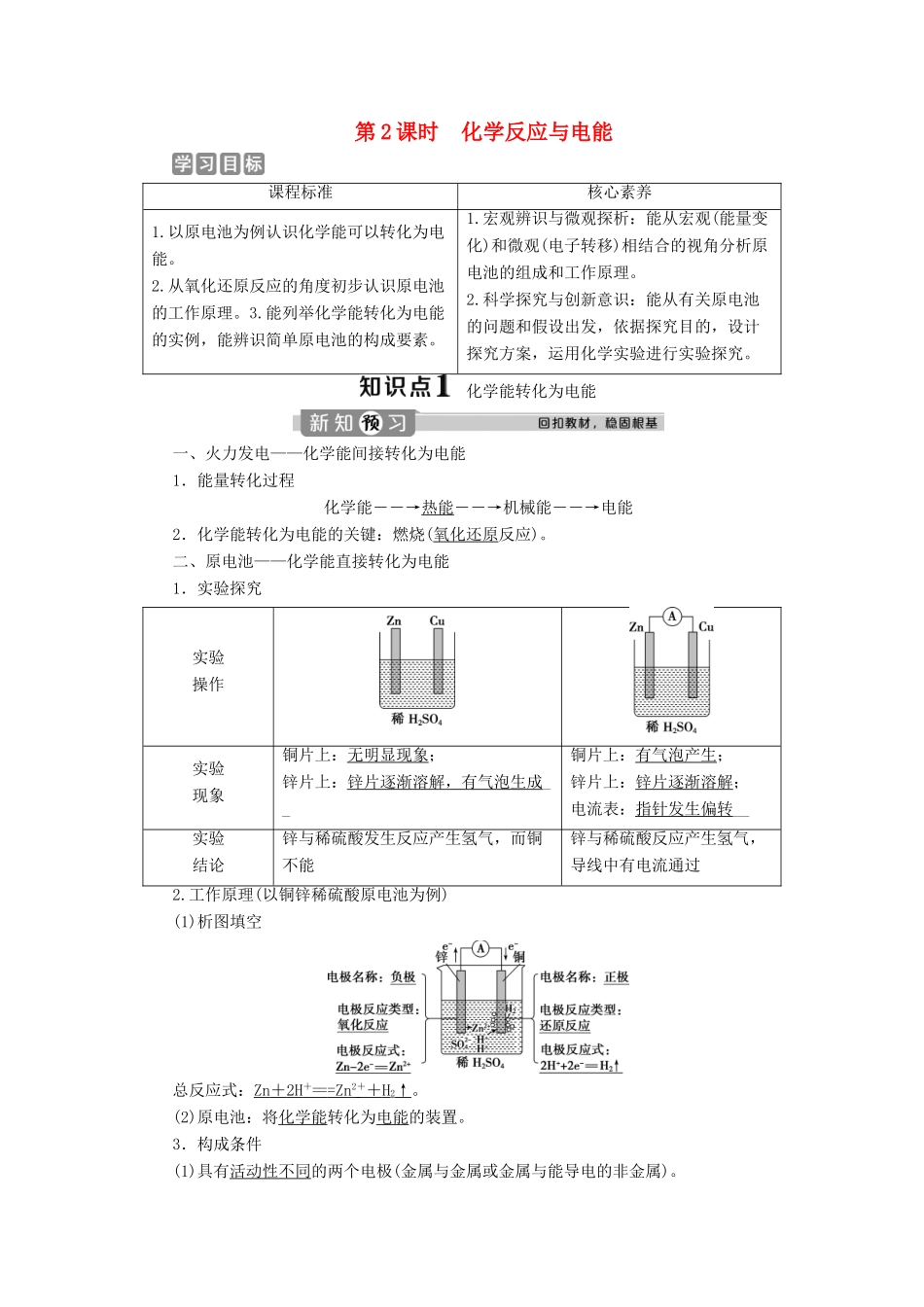
二、原电池——化学能直接转化为电能1.实验探究实验操作实验现象铜片上:无明显现象;锌片上:锌片逐渐溶解,有气泡生成__铜片上:有气泡产生;锌片上:锌片逐渐溶解;电流表:指针发生偏转__实验结论锌与稀硫酸发生反应产生氢气,而铜不能锌与稀硫酸反应产生氢气,导线中有电流通过2
工作原理(以铜锌稀硫酸原电池为例)(1)析图填空总反应式:Zn+2H+===Zn2++H2↑
(2)原电池:将化学能转化为电能的装置
3.构成条件(1)具有活动性不同的两个电极(金属与金属或金属与能导电的非金属)
(2)溶液:两电极均插入电解质溶液中
(3)导线:两电极用导线相连,形成闭合回路
1.多角度判断原电池的正、负极2.原电池原理的应用(1)比较金属活动性原电池中,做负极的金属活动性一般比做正极的金属活动性强
(2)改变化学反应速率如在Zn和稀硫酸反应时,滴加少量CuSO4溶液,则Zn置换出的铜和锌构成原电池的正负极,从而加快Zn与稀硫酸反应的速率
(3)设计原电池如把Fe+2Fe3+===3Fe2+设计成原电池,可用Fe做负极,石墨做正极,FeCl3溶液做电解质溶液
1.下面是有关各种形式能量的相互转化途径的叙述,其中错误的是()A.家庭液化气灶将