第1课时化学反应与热能课程标准核心素养1
认识物质具有能量,认识吸热反应与放热反应
了解化学反应体系能量改变与化学键的断裂和形成有关
知道化学反应可以实现化学能与其他能量形式的转化
体会提高燃料的燃烧效率、开发高能清洁燃料的重要性
变化观念与平衡思想:知道化学变化需要一定条件,并遵循一定规律;认识化学变化的本质是有新物质生成,并伴有能量的转化
宏观辨识与微观探析:能从宏观(反应物和生成物的总能量)和微观(化学键的断裂和形成)相结合的视角分析化学反应中能量的变化
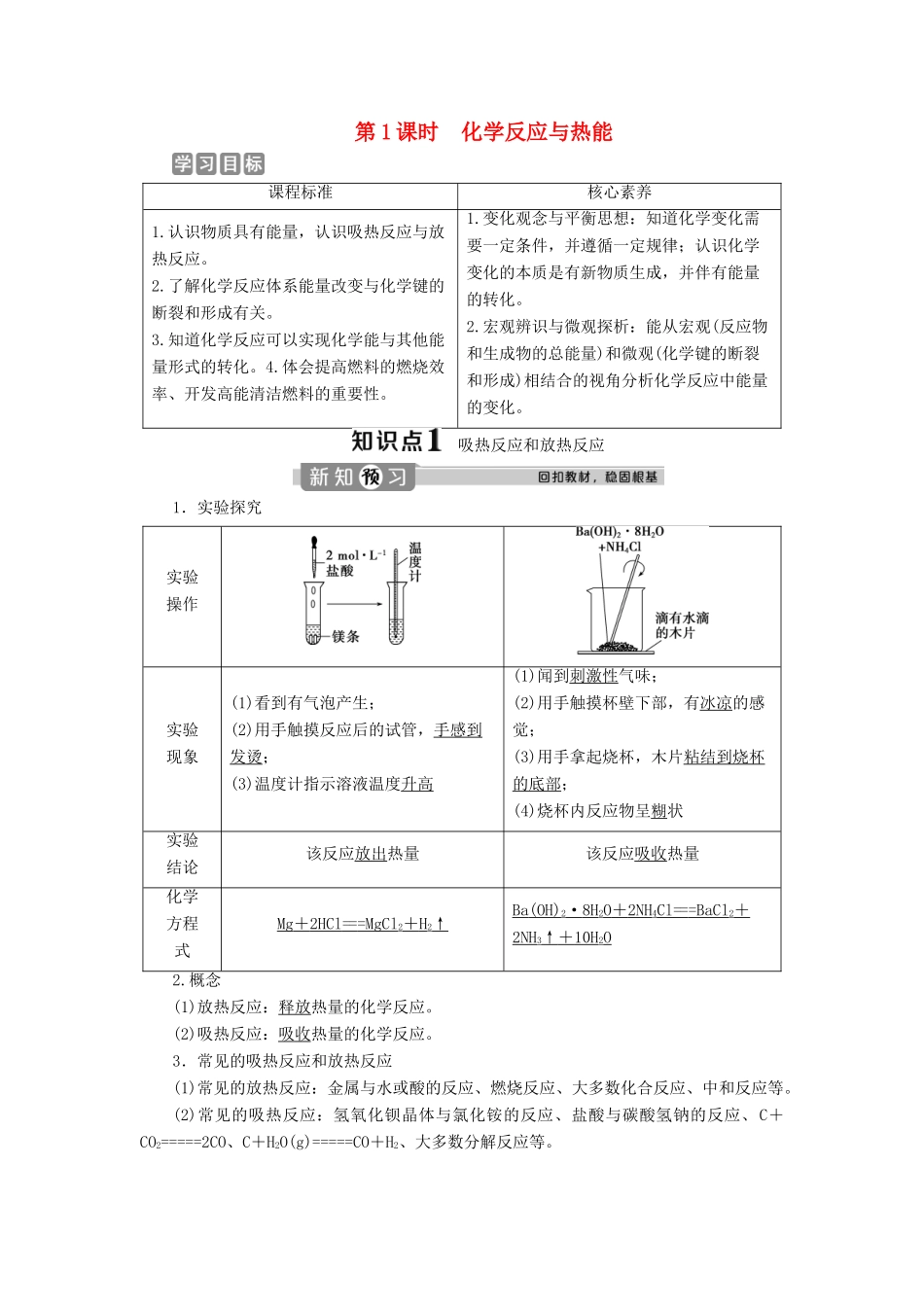
吸热反应和放热反应1.实验探究实验操作实验现象(1)看到有气泡产生;(2)用手触摸反应后的试管,手感到发烫;(3)温度计指示溶液温度升高(1)闻到刺激性气味;(2)用手触摸杯壁下部,有冰凉的感觉;(3)用手拿起烧杯,木片粘结到烧杯的底部;(4)烧杯内反应物呈糊状实验结论该反应放出热量该反应吸收热量化学方程式Mg+2HCl===MgCl2+H2↑Ba(OH)2·8H2O+2NH4Cl===BaCl2+2NH3↑+10H2O2
概念(1)放热反应:释放热量的化学反应
(2)吸热反应:吸收热量的化学反应
3.常见的吸热反应和放热反应(1)常见的放热反应:金属与水或酸的反应、燃烧反应、大多数化合反应、中和反应等
(2)常见的吸热反应:氢氧化钡晶体与氯化铵的反应、盐酸与碳酸氢钠的反应、C+CO2=====2CO、C+H2O(g)=====CO+H2、大多数分解反应等
1.下列反应不一定属于放热反应的是()A.燃烧反应B.H2SO4与Ba(OH)2溶液的反应C.Mg与盐酸的反应D.复分解反应解析:选D
所有燃烧反应、金属与酸的反应、中和反应都属于放热反应,复分解反应则不一定属于放热反应
2.下列反应既属于氧化还原反应,又属于吸热反应的是()A.铝片与稀盐酸的反应B.Ba(OH)2·8H2O与NH4Cl的反应C