第二节元素周期律知识与技能:1、使学生了解元素原子核外电子排布、原子半径、主要化合价与元素金属性、元素非金属性的周期性变化
2、了解两性氧化物和两性氢氧化物的概念
3、认识元素性质的周期性变化是元素原子核外电子排布周期性变化的结果,从而理解元素周期律的实质
4、通过教学,培养学生的逻辑推理能力
过程与方法:1、归纳法、比较法2、培养学生抽象思维能力情感态度价值观:培养学生勤于思考、勇于探究的科学品质
教学重点:原子的核外电子层排布和元素金属性、非金属性变化的规律
教学难点:元素金属性、非金属性变化的规律
教学过程:第1课时设问:碱金属元素间、卤族元素间的化学性质为什么相似
结论:结构决定性质,(性质决定用途)
讲述:目前已发现了100多种元素,它们的结构与性质各有什么联系
这其中有没有什么规律
(引出板书)目前已经发现和合成的115种元素在排列时,也是按一定规律排列的,也有一定的周期,那么,这里面周期是什么
有哪些规律可言
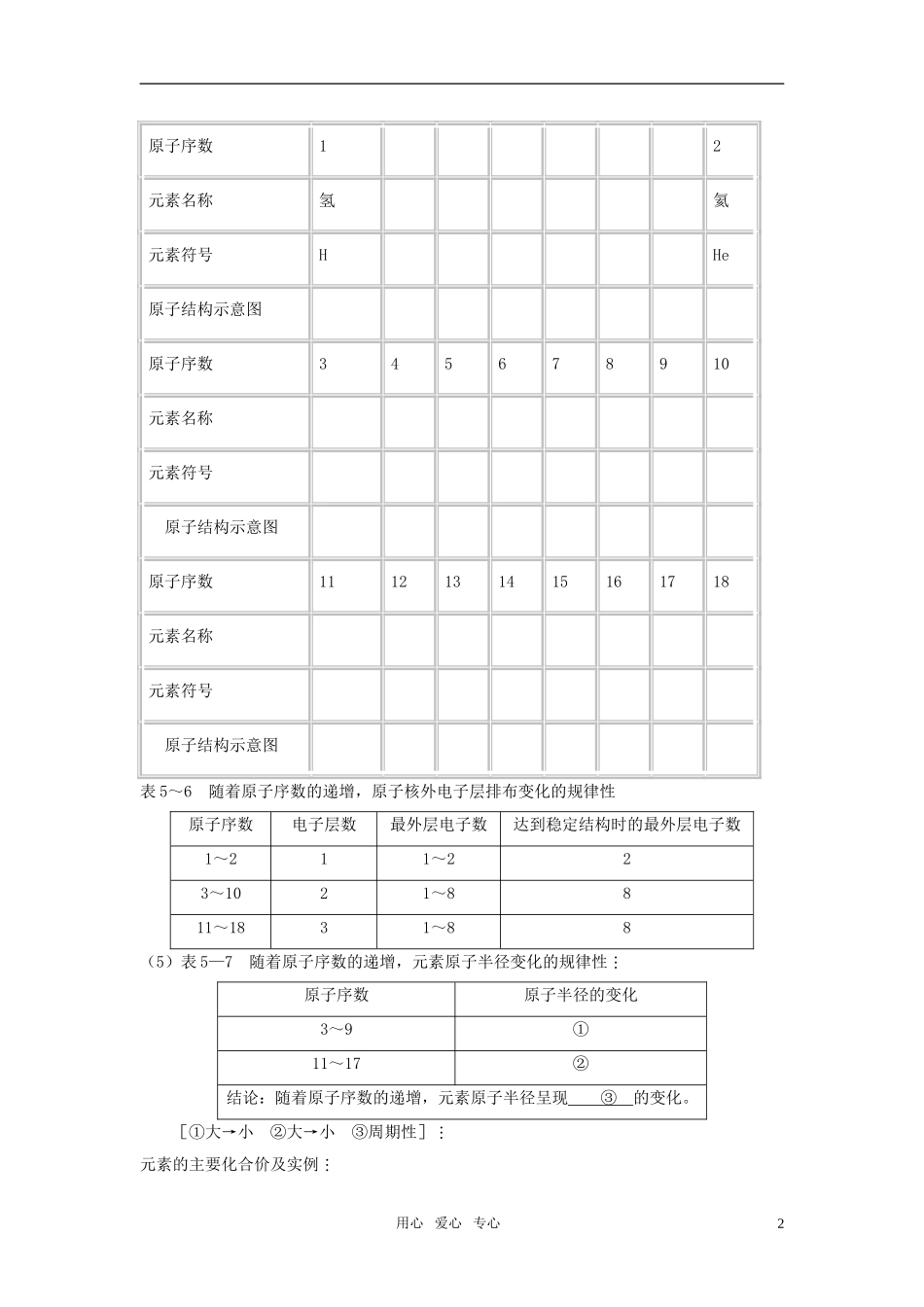
建立原子序数概念后让学生阅读:表5-5、图5-5,解决以下问题:1:原子序数概念:
①随着原子序数的递增,元素的种类呈现怎样的规律性的变化
②随着原子序数递增,原子最外层电子排布呈现怎样规律性变化
③随着原子序数递增,元素原子半径呈现怎样的规律性变化
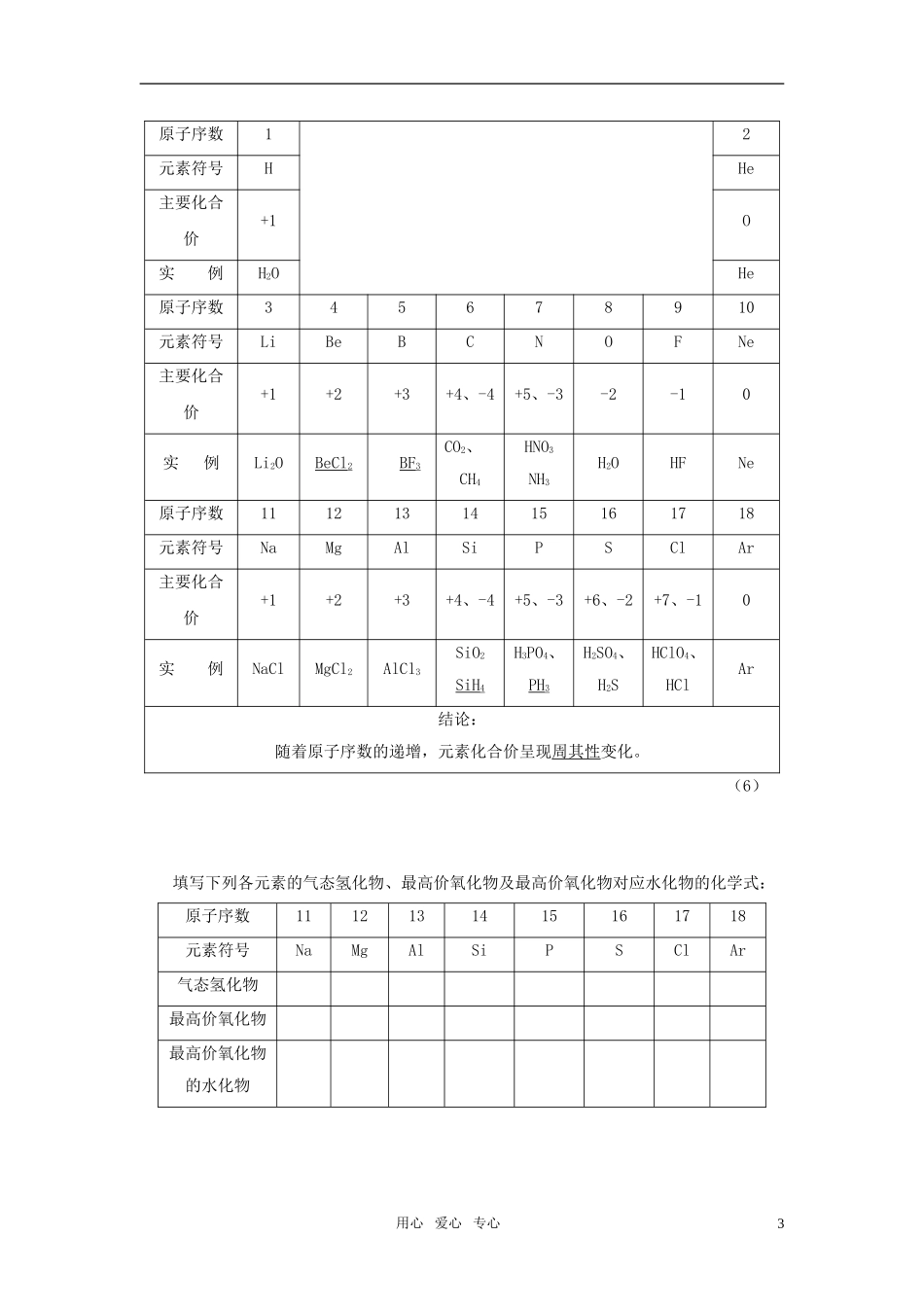
④随着原子序数递增,元素主要化合价呈现怎样的规律性变化
板书:原子序数=核电荷数=质子数=原子核外电子数填表:用心爱心专心1原子序数12元素名称氢氦元素符号HHe原子结构示意图原子序数345678910元素名称元素符号原子结构示意图原子序数1112131415161718元素名称元素符号原子结构示意图表5~6随着原子序数的递增,原子核外电子层排布变化的规律性原子序数电子层数最外层电子数达到稳定结构时的最外层电子数1~211~223~1021~8811~1831~88(5)表5—7随着原子序数的递增,元素原子