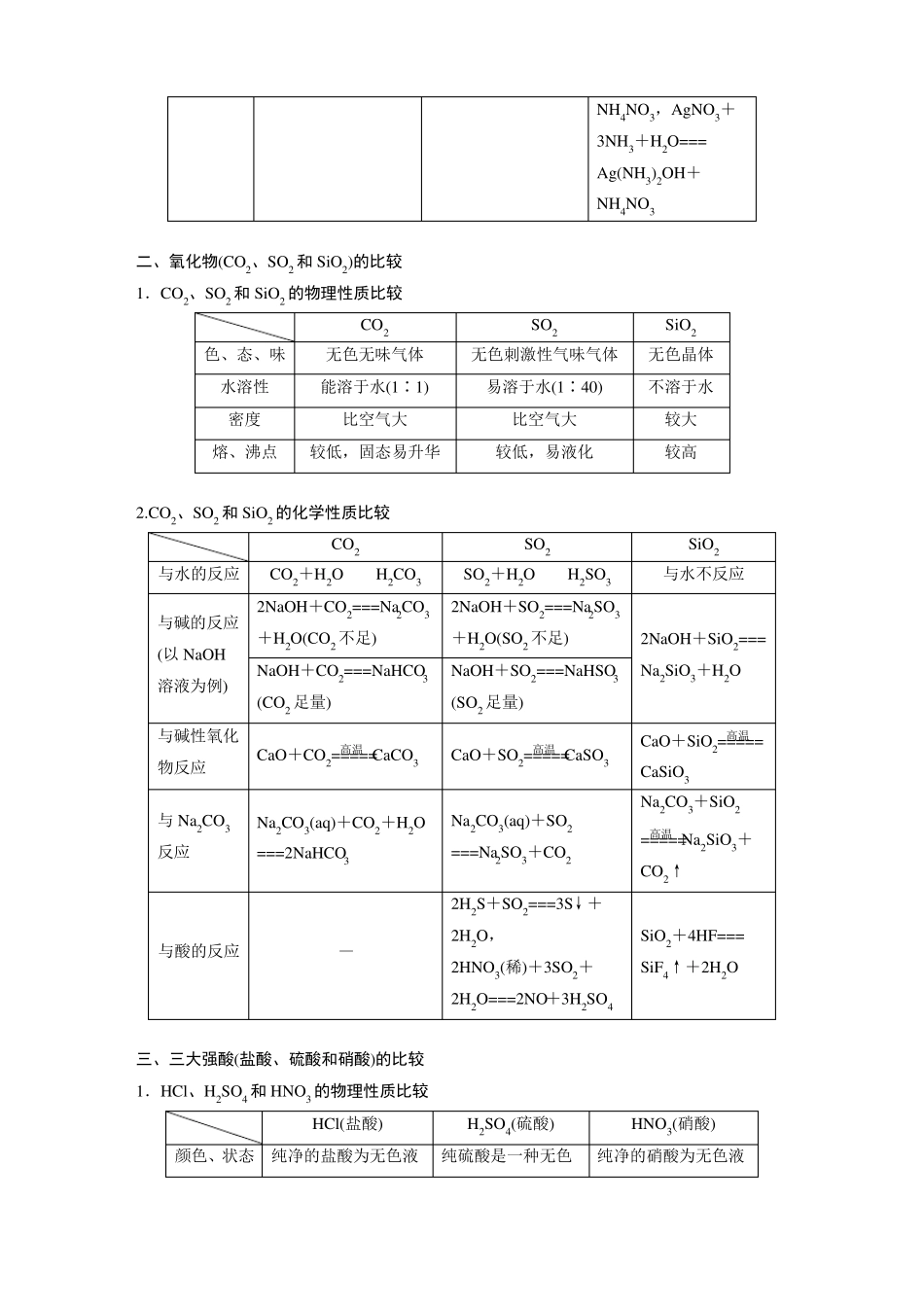
几种重要的物质性质比较一、氢化物(HCl、H2S、NH3)的比较1.HCl、H2S和NH3的制取方法比较HCl利用食盐和浓硫酸在不加热或稍微加热的条件反应原理下,进行反应:NaCl+H2SO4(浓)=====NaHSO4+HCl↑反应装置收集方法尾气处理2
HCl、H2S和NH3的性质比较HCl水溶液显强酸性,与酸碱性碱反应生成盐和水,如NaOH+HCl===NaCl+H2O与活泼金属反应,表氧化性现氧化性,如Fe+2HCl===FeCl2+H2↑与强氧化剂(如MnO2、KClO3等)反还原性H2S水溶液显弱酸性,与碱反应生成盐和水,如2NaOH+H2S===Na2S+2H2O与较活泼金属反应,表现氧化性与较强的氧化剂(如O2、Cl2、SO2等)反应:与某些金属氧化物(氧化剂,如CuO等)反应:3CuO+2NH33Cu+N2+3H2O先生成白色沉淀,氨气过量时,沉淀溶解:AgNO3+NH3+H2O===AgOH↓+NH3水溶液显弱碱性,与酸反应生成盐,如NH3+HCl===NH4Cl固体+液体――→气体向上排空气法用水或碱溶液吸收△△H2S用硫化亚铁跟稀盐酸或稀硫酸反应:FeS+2HCl===FeCl2+H2S↑,FeS+H2SO4(稀)===FeSO4+H2S↑固体+液体―→气体向上排空气法用碱溶液吸收NH3用NH4Cl固体与消石灰混合加热:Ca(OH)2+2NH4Cl=====CaCl2+2NH3↑+2H2O固体+固体――→气体向下排空气法用稀酸溶液吸收△△-△应:MnO2+4HCl(浓)H2S+Cl2=====S↓+=====MnCl2+Cl2↑+2H2O生成白色沉淀:AgNO3+HCl===AgCl↓+HNO3△2HCl,2H2S+SO2===3S↓+2H2O生成黑色沉淀:2AgNO3+H2S===Ag2S↓+2HNO3与AgNO3溶液反应NH4NO3,AgNO3+