化学平衡状态1、概念:化学平衡状态是指在一定条件下的可逆反应里,正反应和逆反应的速率相等,反应混合物中各组分的浓度保持不变的状态
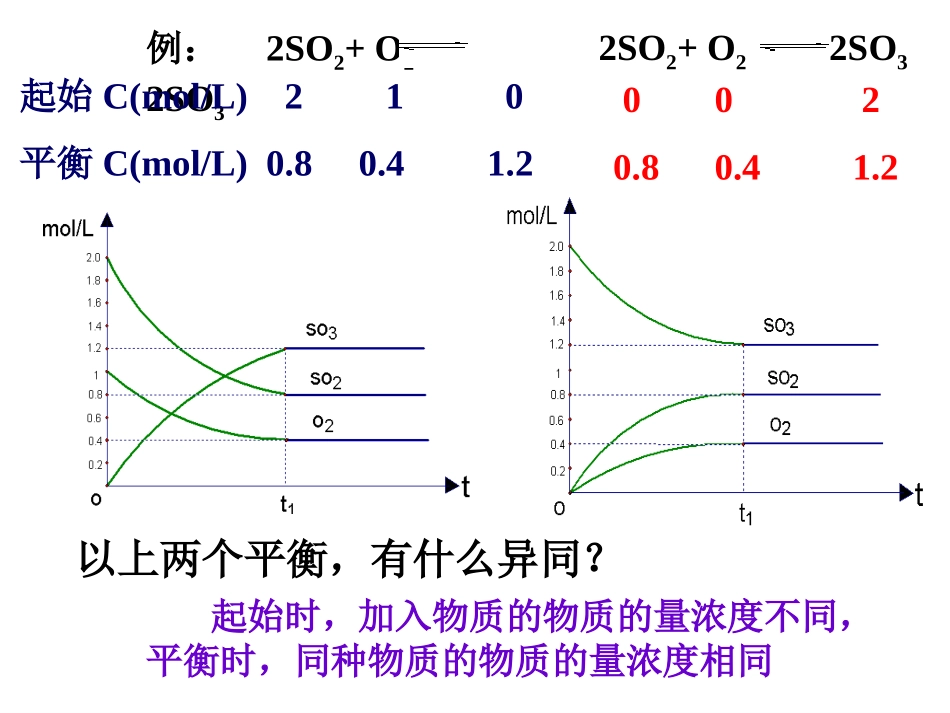
2、特征:逆:研究对象为可逆反应等:V正=V逆判断反应是否处于平衡状态的因素动:V正=V逆≠0动态平衡定:各组分的浓度或其百分含量为定值变:条件变化,化学平衡状态亦发生变化例:2SO2+O22SO3起始C(mol/L)210平衡C(mol/L)0
22SO2+O22SO30020
2以上两个平衡,有什么异同
起始时,加入物质的物质的量浓度不同,平衡时,同种物质的物质的量浓度相同等效平衡:对有气体参加或生成的可逆反应,在一定条件下(恒温恒容或恒温恒压),对同一可逆反应,不论是从正反应开始还是从逆反应开始,只是起始时加入物质的物质的量不同,而达到化学平衡时,同种物质的百分含量相同(体积分数、物质的量分数、或质量分数),这样的平衡称为等效平衡
等效平衡的判断方法任何状态的体系,都用“极端状态”来比较,只要能转化为相同的“极端状态”,就一定是等效平衡
途径1起始CO+H2OCO2+H22mol1mol00途径2起始途径3起始途径4起始4mol2mol001mol01mol1mol1
5molT、V不变或T、P不变时:转化到一边物质的量完全相同或比例完全相同N2(g)+3H2(g)2NH3(g)T、V不变途径1起始途径2起始途径3起始1mol4mol001mol2mol0
5mol1mol规律:转化到一边物质的量或浓度完全相同N2(g)+3H2(g)2NH3(g)T、P不变途径1起始途径2起始途径3起始1mol4mol00
5mol2mol00
5mol1mol途径4起始1mol5mol2mol规律:转化到一边物质的量或浓度比例完全相同练习1、有一个固定体积的密闭容器中,加