第一节金属的化学性质第三章金属及其化合物知识回顾:1、金属有哪些物理性质
不透明,有金属光泽,良好的导电、导热性、延展性……2、金属能发生哪些化学反应
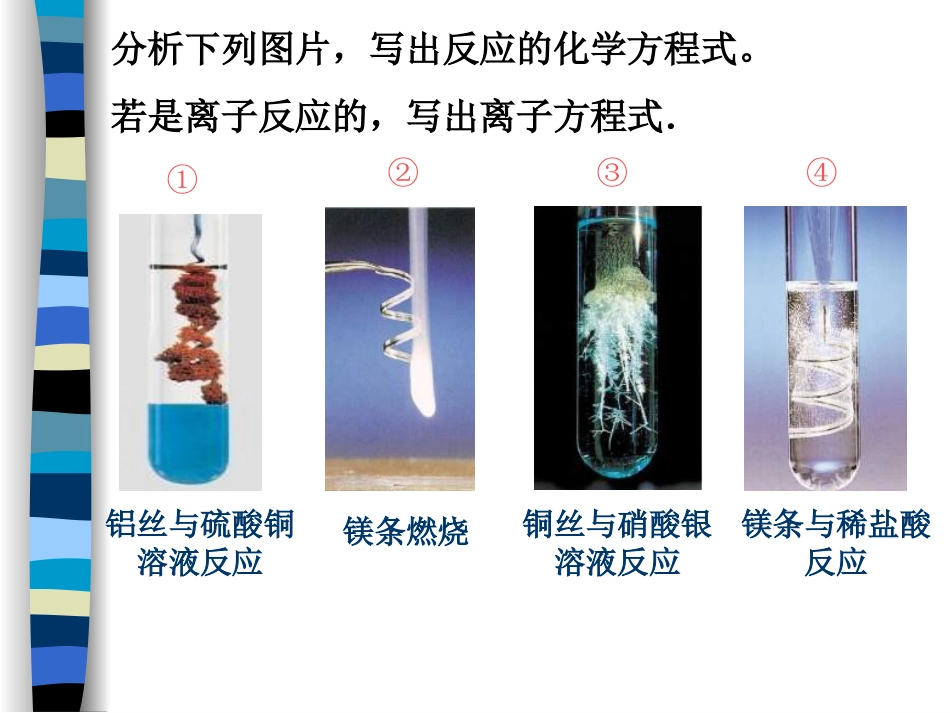
与氧气、酸、盐溶液反应……分析下列图片,写出反应的化学方程式
若是离子反应的,写出离子方程式.①铝丝与硫酸铜溶液反应②镁条燃烧③铜丝与硝酸银溶液反应④镁条与稀盐酸反应①2Al+3Cu2+=2Al3++3Cu②不是
③Cu+2Ag+=Cu2++2Ag④Mg+2H+=Mg2++H2↑3、依据Na、Mg、Al的原子结构示意图,分析它们的原子结构有什么特点,与金属的化学性质有什么联系
NaMgAl金属最外层上的电子一般少于4个,反应中很容易失去电子,表现出较强的还原性
(做还原剂)金属具备一定的失电子能力,因此有一定的还原性,根据活动性顺序,排在越前的金属越活泼,越容易失去电子,还原性也越强
【实验1】用镊子取一小块金属钠,用滤纸吸干表面的煤油,用小刀切去一端的表层,观察表面的颜色一、钠(一)、物理性质钠的化学性质怎么样
取决于什么呢
一、钠银白色固体,质软,密度比水小、比煤油大,熔沸点低,能导电导热
Na的原子结构示意图在化学反应中,Na很容易失去最外层的一个电子,形成Na+,表现出还原性NaNa+失去e-推测:金属钠的化学性质很活泼取一小块金属钠,用滤纸吸干表面的煤油,用小刀切去一端的表层,观察表面的颜色;将其放置在空气中,观察表面颜色的变化
反应:4Na+O2==2Na2O现象:钠的新切面由光亮的银白色渐渐变暗【实验2】将一小块金属钠放在石棉网上,用酒精灯对其加热,观察实验现象
反应:2Na+O2===Na2O2(淡黄色)△现象:钠在空气中受热后,先熔化成闪亮的小球后剧烈燃烧产生黄色火焰,生成淡黄色固体
-1(一)物理性质一、钠(二)化学性质1
与非金属单质反应(O2、Cl2)(1)Na与O2反应常温下,4Na+O2==2Na