第二节化学能与电能第一课时——原电池一、原电池1
定义:将化学能直接转变成电能的装置,称为原电池电源2
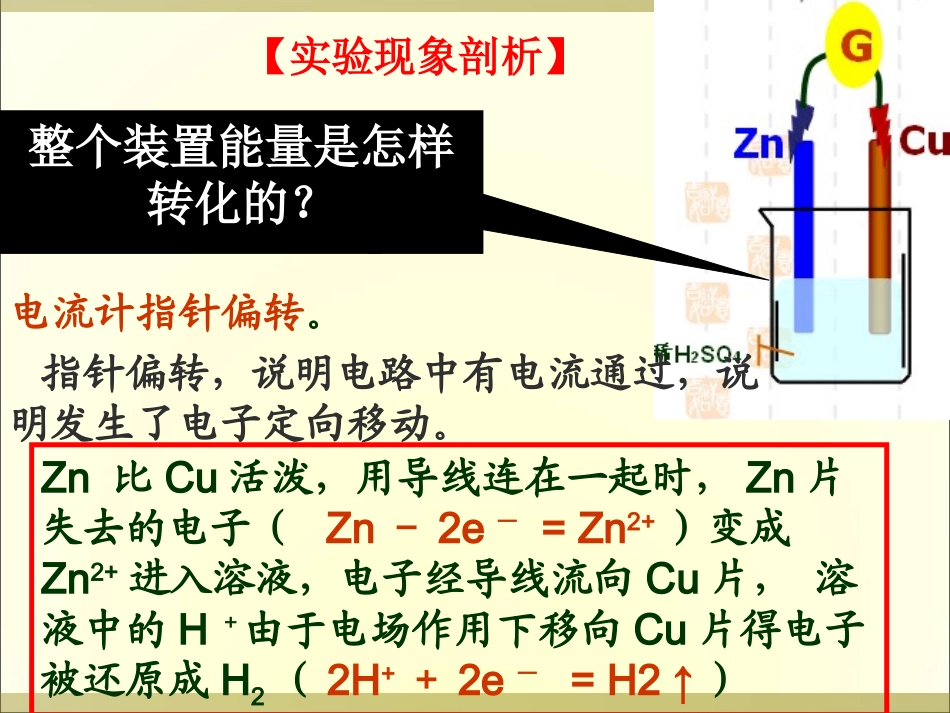
正负极:+-负极:电子流进(或电流流出)的一极正极:电子流出(或电流流进)的一极【实验现象剖析】Zn片逐渐溶解但无气泡;Cu片上有气泡(H2);电流计指针偏转
指针偏转,说明电路中有电流通过,说明发生了电子定向移动
Zn比Cu活泼,用导线连在一起时,Zn片失去的电子(Zn-2e-=Zn2+)变成Zn2+进入溶液,电子经导线流向Cu片,溶液中的H+由于电场作用下移向Cu片得电子被还原成H2(2H++2e-=H2↑)整个装置能量是怎样转化的
一、原电池3
电极反应:电极材料原电池正负极电极反应式发生的反应Zn片Cu片电极总离子反应负极正极Zn-2e-=Zn2+2H++2e-=H2↑氧化反应还原反应Zn+2H+=Zn2++H2↑(两个电极反应之和)小结:负极失去电子的一极氧化反应活性强正极得到电子的一极还原反应活性弱e-↑e-→e-↓⊕_外电路:内电路:阳离子→正极阴离子→负极负极→正极e-这样整个电路构成了闭合回路,带电粒子的定向移动产生电流一、原电池4
工作原理:正极→负极ⅠH2SO4(aq)CuSO4(aq)ZnCu负极():
课堂练习:请在图上标出电子的流动方向和电流方向,并判断正负极,写出电极反应式和总反应式
AgFeIe-e-IFeAgFe-2e-=Fe2+2H++2e-=H2↑Fe+2H+=Fe2++H2↑ZnCuZn-2e-=Zn2+Cu2++2e-=CuZn+Cu2+=Zn2++CuAAAAAAZnCuFeC(石墨)ZnCuZnZnFeCuSiC(石墨)稀H2SO4CuSO4溶液稀H2SO4稀H2SO4ABCDZnCuA稀H2SO4酒精稀H2SO4EFG√√√××××一、原电池5
原电池的形成条件:两