第二节影响化学反应速率的因素影响化学反应速率的因素不同化学反应的速率反应物本身性质(内因)同一化学反应的速率外界条件(外因)内因——物质本身的性质(决定性因素)探究实验2-2浓度对化学反应速率的影响0
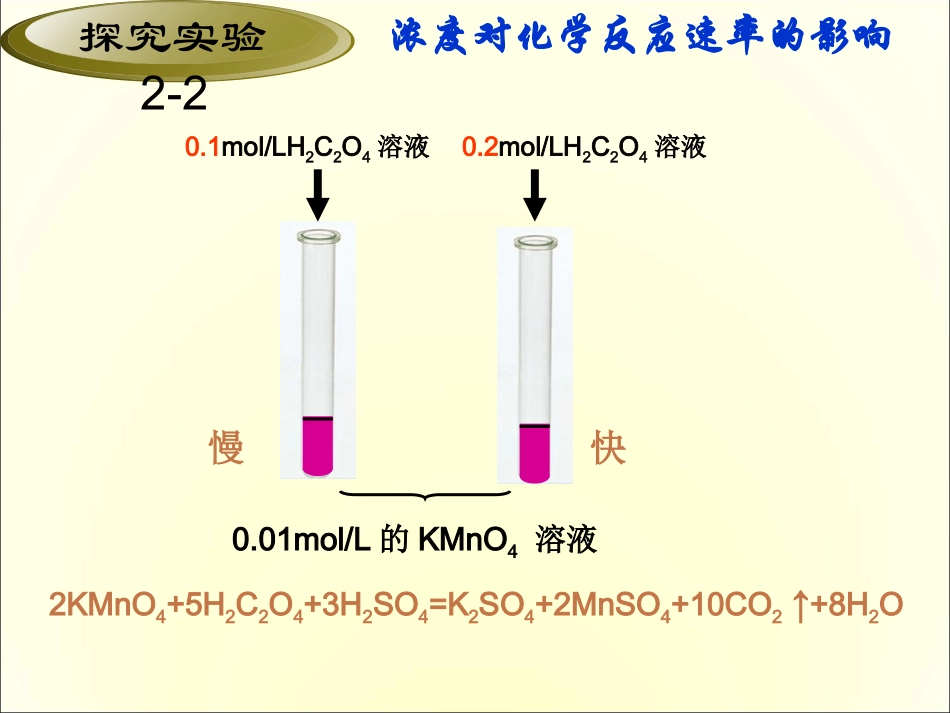
01mol/L的KMnO4溶液0
1mol/LH2C2O4溶液0
2mol/LH2C2O4溶液快慢2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O结论:其它条件相同时,增加反应物的浓度,反应速率加快;反之,降低反应物的浓度,反应速率减慢
注意增加固体物质或纯液体的量,因其浓度是个定值,故不影响反应速率(不考虑表面积的影响)
如反应:3KSCN+FeCl3=Fe(SCN)3+3KCl若在上述反应体系中加入KCl晶体,不会影响化学反应速率
巩固练习因为反应实质为:Fe3++3SCN-=Fe(SCN)3不会探究实验2-3温度对化学反应速率的影响5mL0
1mol/L的H2SO4+5mL0
1mol/LNa2S2O3热水冷水快慢Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O结论:其它条件相同时,升高温度,反应速率加快;反之,降低温度,反应速率减慢
科学探究已知:4H++4I-+O2=2I2+2H2O现有1mol/LKI溶液、0
1mol/LH2SO4溶液和淀粉溶液,请设计实验探究溶液出现蓝色的时间与温度的关系
【结论】其它条件相同时,温度高,出现蓝色的时间短;温度低,出现蓝色的时间长
一般来说,温度每升高10℃,反应速率增大到原来的2~4倍
探究实验催化剂对化学反应速率的影响2H2O22H2O+O2↑MnO2【结论】其它条件不变时,选用适当的催化剂可以改变反应速率;正催化剂使反应速率加快,负催化剂使反应速率减慢
科学探究〖探究1〗设计实验比较在2mL5%的H2O2中加入FeCl3和CuSO4溶液各1mL,比较二者分解速率