实验探究请根据反应:Zn+CuSO4=ZnSO4+Cu设计一个原电池实验探究1CuSO4溶液电流表指针发生偏转吗
指针稳定吗
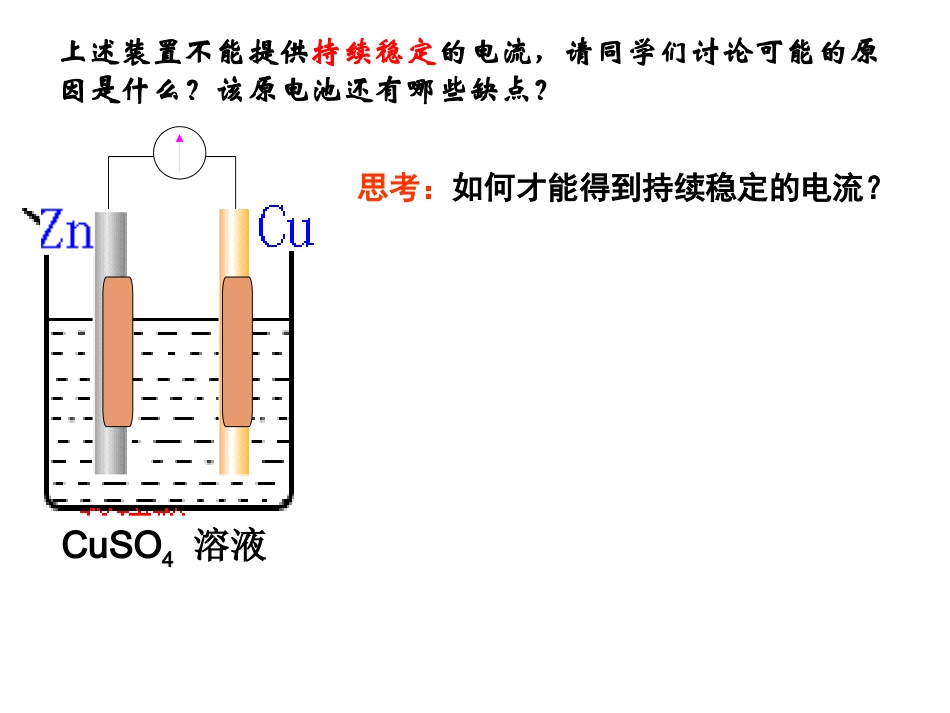
两个电极上都有什么现象
实验探究2该装置是否构成原电池
电流表指针发生偏转吗
铜电极上有什么现象
CuSO4溶液思考:如何才能得到持续稳定的电流
上述装置不能提供持续稳定的电流,请同学们讨论可能的原因是什么
该原电池还有哪些缺点
ZnSO4溶液CuSO4溶液ZnCu
改进CuSO4CuZnAA盐桥中装有饱和的KCl溶液和琼脂制成的胶冻,胶冻的作用是防止管中溶液流出
铜锌原电池盐桥的作用:(1)形成闭合回路
(2)平衡电荷
将化学能转变为电能的装置将化学能转变为电能的装置1
组成——两个半电池、盐桥②使两个烧杯中的溶液连成一个通路盐桥的作用盐桥的作用①让溶液始终保持电中性使电极反应得以继续进行一、原电池2、工作原理内电路:Zn原子失去电子成为Zn2+进入溶液,使ZnSO4溶液因Zn2+增加而带正电,盐桥中的Cl—会移向ZnSO4溶液;同时Cu2+获得电子成为金属沉淀在铜片上,使CuSO4溶液因SO42—相对增加而带负电,盐桥中的K+移向CuSO4溶液,从而形成闭合回路
外电路:Zn失去电子沿导线通过电流表进入铜片Zn——负极Cu2eCu2Cu——正极Zn-2e-=Zn2+总反应方程式:Zn+Cu2+=Zn2++Cu3、电极反应将原电池反应中的氧化反应与还原反应分开在两个不同区域内进行,再以适当的方式连接起来,从而获得了稳定持续的电流
改进后的原电池装置还有什么优点