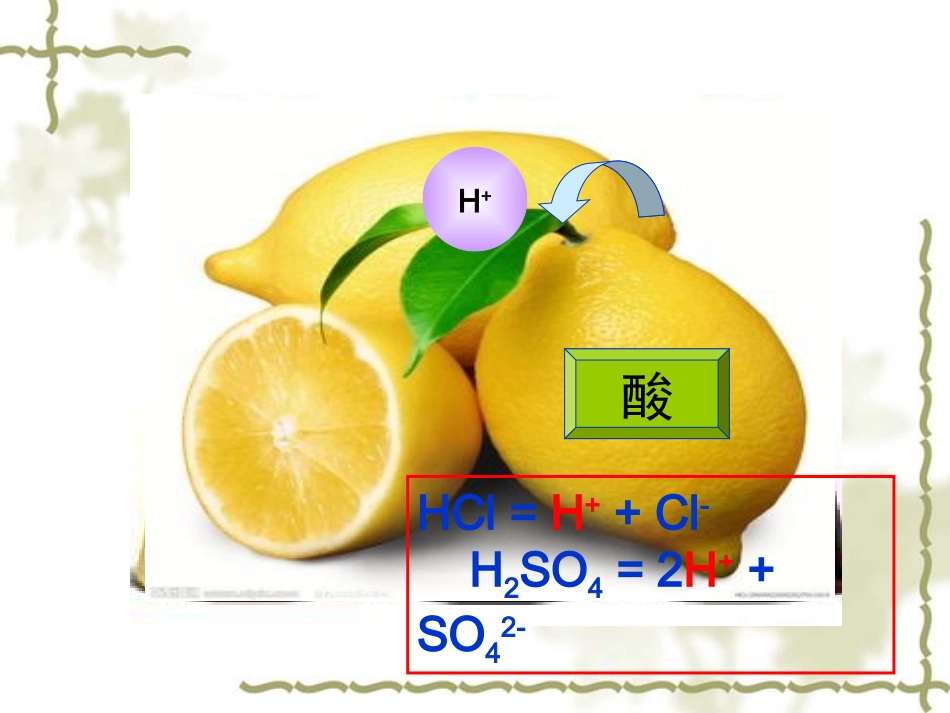
H+HCl=H++Cl-H2SO4=2H++SO42-酸探究浓硫酸和浓盐酸的物理性质观察浓硫酸和浓盐酸的状态、颜色,比较它们与同体积水的质量大小,打开瓶塞,观察发生的现象;闻一闻是否有气味
注意:闻气体的方法浓盐酸(37~38%)Hydrochloricacid500ml密度(1
19g/mL)化学式HCl相对分子质量36
5符合GB622-89腐蚀品浓硫酸(98%)Sulfuricacid500ml密度(1
84g/mL)化学式H2SO4相对分子质量98符合GB622-89腐蚀品无色无色液态刺激性液态H2H20H2浓硫酸的特性吸水性脱水性强氧化性强腐蚀性浓硫酸的稀释浓硫酸沿着器壁慢慢注入水中,而且要不断搅拌
稀释浓硫酸的方法:动画演示加深印象
点拔:水的密度较小,浮在浓硫酸上面,溶解时放出大量热,使水立刻沸腾,使硫酸液滴向四周飞溅,这是非常危险的
稀释浓硫酸时,一定要把浓硫酸沿着器壁慢慢注入水里,并不断搅拌
切不可将水倒进浓硫酸里
使用浓硫酸注意的问题:1、浓硫酸的稀释方法:2、少量浓硫酸溅到皮肤上的处理方法:应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液浓硫酸和浓盐酸的物理性质浓硫酸浓盐酸溶质的化学式H2SO4HCl颜色状态气味密度1
84g·cm-31
19g·cm-3打开瓶塞时的现象溶质质量分数98%37%~38%其它特性无色无色无色透明液体粘稠油状的液体有刺激性气味瓶口有白雾出现无现象无味易挥发、强腐蚀性有吸水性(作干燥剂)、脱水性、强氧化性、强腐蚀性把一定质量的浓盐酸和浓硫酸分别敞口放置于空气中一段时间(忽略水分的蒸发)变化的结果是:填“增大”“减小”或“不变”
溶质的质量溶剂的质量溶液的质量溶质质量分数浓盐酸浓硫酸减小不变不变增加减小增加减小减小实验内容反应现象化学方程式稀盐酸紫色石蕊试液无色酚酞试液镁条生锈铁钉碳酸钠硝酸银溶液氯化钡溶液紫色石蕊试液变红