[江苏考纲要求]————————————————————————————————————1.熟悉常见元素的化合价
能根据化合价正确书写化学式(分子式),或根据化学式判断元素的化合价
2.理解氧化还原反应的本质,了解氧化还原反应在生产、生活中的应用
3.掌握常见氧化还原反应的配平和相关计算
[教材基础—自热身]1.本质和特征氧化还原反应的本质是电子转移(得失或偏移),特征是反应过程中元素的化合价发生变化
2.相关概念及其关系例如,反应MnO2+4HCl(浓)=====MnCl2+Cl2↑+2H2O中,氧化剂是MnO2,还原剂是HCl,氧化产物是Cl2
生成1molCl2时转移电子数目为2NA,被氧化的HCl的物质的量是2_mol,HCl显示的性质是还原性和酸性
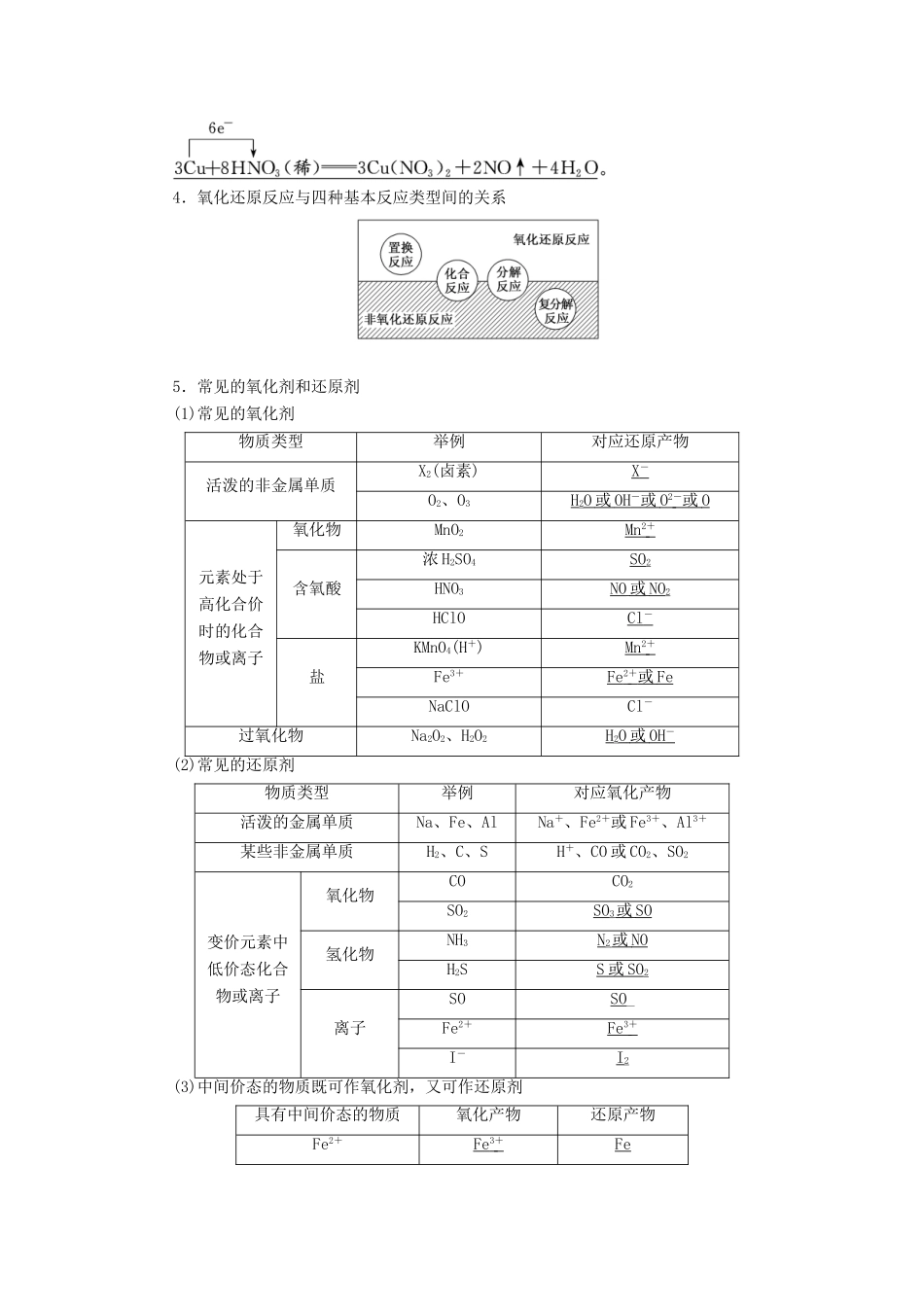
3.氧化还原反应中电子转移的表示方法(1)双线桥法例如:写出Cu与稀硝酸反应的化学方程式并用双线桥标出电子转移的方向和数目:_______________________________________________________________
(2)单线桥法例如:写出Cu与稀硝酸反应的化学方程式并用单线桥标出电子转移的方向和数目:氧化还原反应的相关概念及电子转移表示法4.氧化还原反应与四种基本反应类型间的关系5.常见的氧化剂和还原剂(1)常见的氧化剂物质类型举例对应还原产物活泼的非金属单质X2(卤素)X-O2、O3H2O或OH-或O2-或O元素处于高化合价时的化合物或离子氧化物MnO2Mn2+含氧酸浓H2SO4SO2HNO3NO或NO2HClOCl-盐KMnO4(H+)Mn2+Fe3+Fe2+或FeNaClOCl-过氧化物Na2O2、H2O2H2O或OH-(2)常见的还原剂物质类型举例对应氧化产物活泼的金属单质Na、Fe、AlNa+、Fe2+或Fe3+、Al3+某些非金属单质H2、C、SH+、CO或CO2、SO