电化学本讲主要从三个方面归纳电化学的基本内容
一是正确区别原电池、电解池和电镀池,二是掌握原电池,电解规律及应用,三是有关电化学基本计算的方法及技能
基础知识学习指导1
怎样区别原电池、电解池
试从组成、原理、能量转化等方面进行比较
项目原电池电解池能量转换化学能转变为电能电能转变为化学能实质氧化还原反应产生电流在电流作用下发生氧化还原反应形成条件活泼性不同的两种导体,插入电解质溶液中形成闭合回路与外加电源相连接的两个电极插入电解质溶液中判别无外加电源有外加直流电源电极判断负极:相对活泼的电极正极:较不活泼的电极阳极:与电源正极相连的一极阴极:与电源负极相连的一极电极反应负极:失去电子发生氧化反应M-ne-=Mn+正极:阳离子得电子发生还原反应Rm++me-=R阳极:金属阳极或溶液中较易失去电子的阴离子发生氧化反应M-ne-=Mn+或Mn--ne-=M阴极:溶液中轻易得电子的阳离子发生还原反应解析1Rm++me-=R电子流向负极→经外电路→正极电源负极→导线→阴极→阳离子被还原→溶液中阴离子→阳极→失去电子→电源正极电解液变化电解液成分发生变化电解液成分不一定变化,溶液的pH值可能变化解析2图例2
什么是电化腐蚀
怎样防护金属的腐蚀
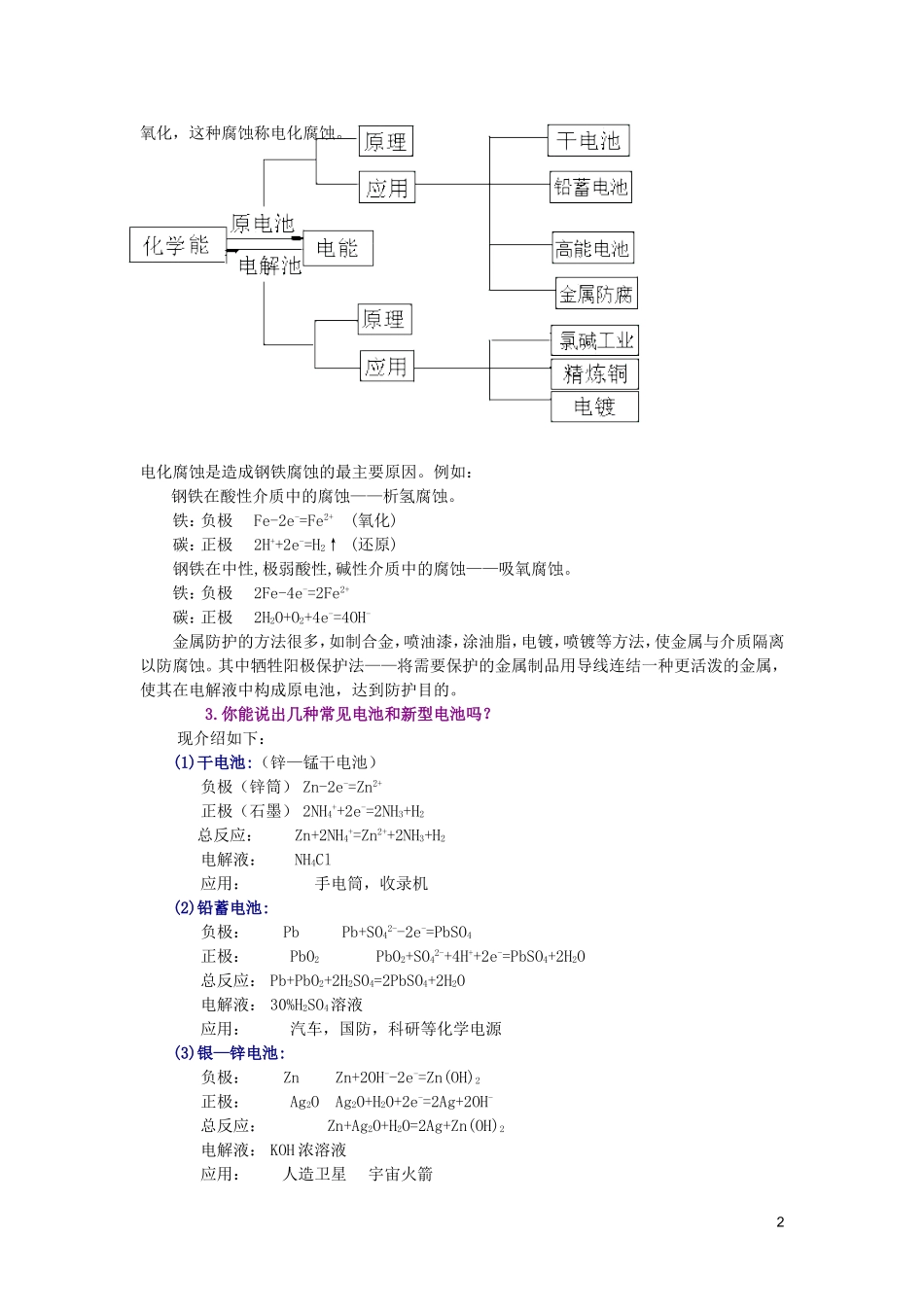
不纯的金属或合金与电解液接触时,会发生原电池反应,比较活泼的金属失去电子而被1氧化,这种腐蚀称电化腐蚀
电化腐蚀是造成钢铁腐蚀的最主要原因
例如:钢铁在酸性介质中的腐蚀——析氢腐蚀
铁:负极Fe-2e-=Fe2+(氧化)碳:正极2H++2e-=H2↑(还原)钢铁在中性,极弱酸性,碱性介质中的腐蚀——吸氧腐蚀
铁:负极2Fe-4e-=2Fe2+碳:正极2H2O+O2+4e-=4OH-金属防护的方法很多,如制合金,喷油漆,涂油脂,电镀,喷镀等方法,使金属与介质隔离以防腐蚀
其中牺牲阳极保护法——将需要保护的金属制品用导线连结一种更活泼的金