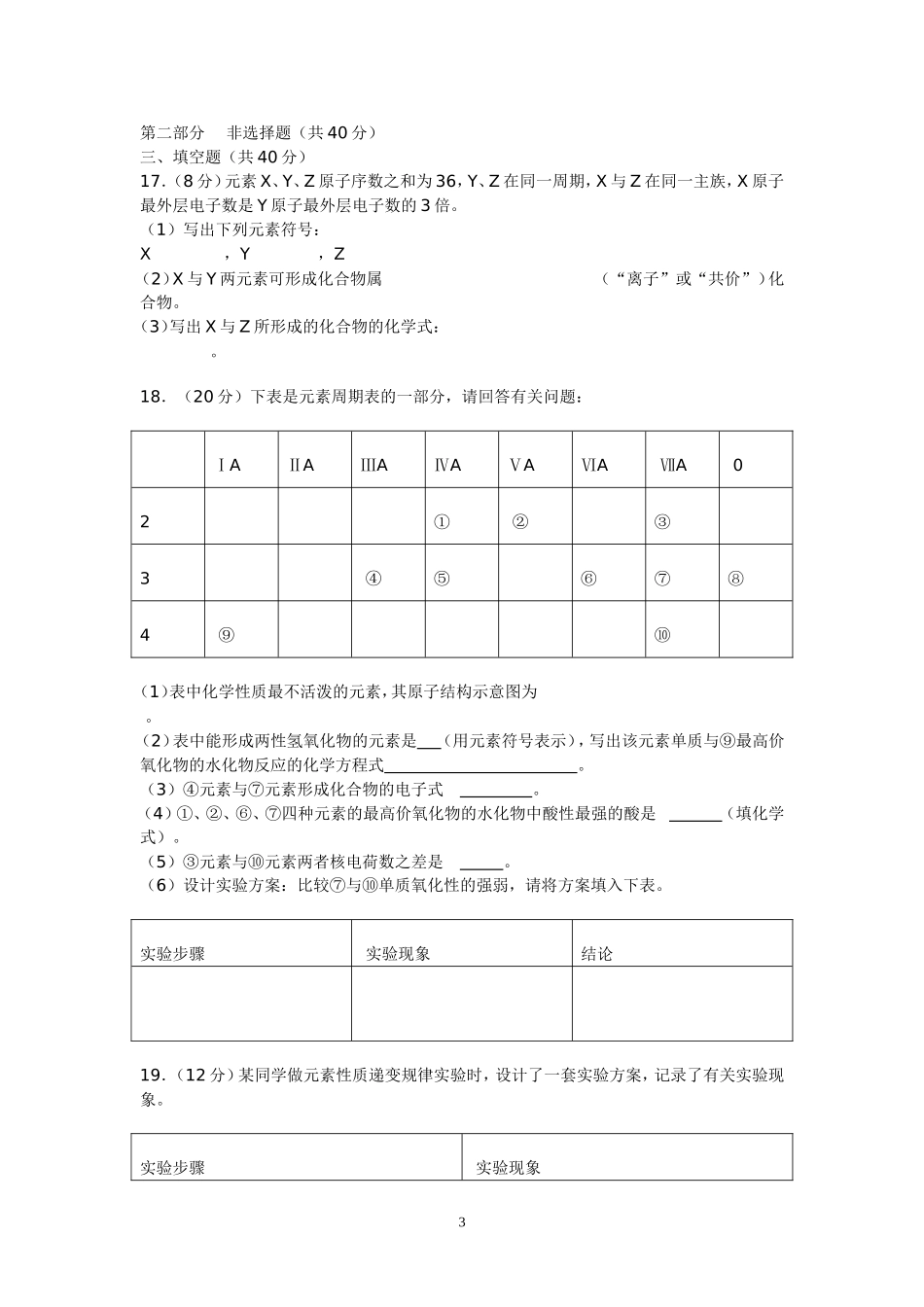
第一章《物质结构元素周期律》测试题班级姓名第一部分选择题(共60分)一、单项选择题(共10小题,每小题3分,共30分。)1.下列元素中,不属于主族元素的是A.钾B.铁C.碘D.硅2.下列关于放射性气体氡22286Rn的说法正确的是A.质量数为222B.中子数为86C.质子数为136D.核电荷数为2223.元素周期表中某区域的一些元素多用于制造半导体材料,它们是A.左下方区域的金属元素B.右上方区域的非金属元素C.稀有气体元素D.金属元素与非金属元素分界线附近的元素4.下列有关元素周期律的叙述中,正确的是A.氧化性强弱:F2<Cl2B.金属性强弱:K<NaC.酸性强弱:H3PO4<H2SO4D.碱性强弱:NaOH<Mg(OH)25.下列各组三种元素中,属于同一周期的是A.C、H、OB.F、Cl、BrC.Li、Mg、BD.Si、S、P6.下列物质中含离子键的是A.HClB.NaFC.CH4D.NH37.第三周期R元素的原子,其次外层的电子数为最外层电子数的2倍,则R是A.LiB.SC.SiD.P8.下列关于周期表的说法正确的是A.同一周期元素原子的最外层电子数相同B.同一主族元素原子的电子层数相同C.能生成碱的金属都在第ⅠA族D.第ⅦA族元素统称为卤族元素9.按钠、钾、铷、铯的顺序,下列有关叙述正确的是A.其氢氧化物中碱性最强的是NaOHB.单质还原能力最强的是钠原子C.单质的熔点逐渐增大D.原子半径随核电荷数的增大而增大10.下列关于元素周期表的叙述正确的是A.周期表中有八个A族,八个B族B.目前使用的元素周期表中,最长的周期含有32种元素C.短周期元素是指1-20号元素D.原子及其离子的核外电子层数都等于该元素所在的周期数1二、多项选择题(共6小题,每小题5分,共30分。每小题至少有2个选项正确,少选且正确得2分,错选、未选不得分)11.下列关于32He的说法正确的是A.32He原子核内含有2个中子B.32He原子核内含有2个质子C.32He原子核外有3个电子D.32He和42He是两种不同的核素12.下列有关原子结构和元素周期律表述正确的是A.ⅦA族元素是同周期中非金属性最强的元素B.原子序数为15的元素的最高化合价为+3C.原子序数为12的元素位于元素周期表的第三周期ⅡA族D.第二周期ⅣA族元素的原子核电荷数和中子数一定为613.下列事实能用来判断非金属性强弱依据的是A.单质的熔点、沸点高低B.非金属之间发生的置换反应C.非金属与氢气生成气态氢化物的难易程度D.非金属元素的最高价氧化物的水化物的酸性强弱14.Y元素的阳离子和X元素的阴离子具有与氩原子相同的电子层结构,下列叙述正确的是A.Y的原子序数比X的大B.Y的原子半径比X的大C.Y原子的最外层电子数比X的大D.Y元素的最高正价比X的大15.同周期的X、Y、Z三种元素,它们的气态氢化物的化学式分别为H2X、YH3、ZH4,下列说法正确的是A.气态氢化物的稳定性按X、Y、Z的顺序递增B.三种元素的最高价氧化物对应的水化物酸性:H2ZO3>H3YO4>H2XO4C.元素的最高正化合价按X、Y、Z的顺序递减D.元素原子的半径按X、Y、Z的顺序递增16.下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是元素代号LMRT原子半径/nm0.1600.1430.1020.074主要化合价+2+3+6、-2-2A.L2+与R2-的核外电子数相等B.M与T形成的化合物具有两性C.气态氢化物的稳定性为H2T<H2RD.L和M金属性强弱比较:L>M2第二部分非选择题(共40分)三、填空题(共40分)17.(8分)元素X、Y、Z原子序数之和为36,Y、Z在同一周期,X与Z在同一主族,X原子最外层电子数是Y原子最外层电子数的3倍。(1)写出下列元素符号:X,Y,Z(2)X与Y两元素可形成化合物属(“离子”或“共价”)化合物。(3)写出X与Z所形成的化合物的化学式:。18.(20分)下表是元素周期表的一部分,请回答有关问题:ⅠAⅡAⅢAⅣAⅤAⅥAⅦA02①②③3④⑤⑥⑦⑧4⑨⑩(1)表中化学性质最不活泼的元素,其原子结构示意图为。(2)表中能形成两性氢氧化物的元素是(用元素符号表示),写出该元素单质与⑨最高价氧化物的水化物反应的化学方程式。(3)④元素与⑦元素形成化合物的电子式。(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的酸是(填化学式)。(5)③元素与⑩元素两者核电荷数...