倍速课时学练倍速课时学练第十单元酸和碱课题1常见的酸和碱倍速课时学练倍速课时学练倍速课时学练第一课时生活中的一些物质含有酸食醋中含有醋酸汽车用铅蓄电池中含有硫酸柠檬、柑橘等水果中含有柠檬酸倍速课时学练倍速课时学练倍速课时学练回忆:1、把二氧化碳通入紫色石蕊的试管中会看到什么现象
该现象说明了什么
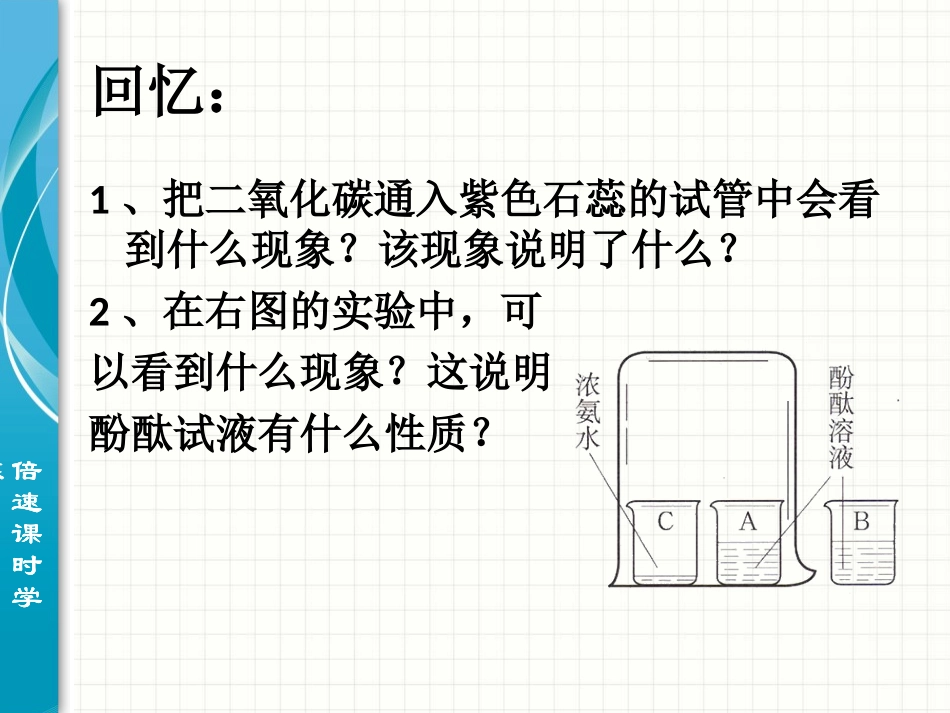
2、在右图的实验中,可以看到什么现象
这说明酚酞试液有什么性质
倍速课时学练倍速课时学练倍速课时学练加入紫色石蕊溶液后的颜色变化加入无色酚酞溶液后的颜色变化食醋石灰水盐酸氢氧化钠酸碱指示剂与酸、碱的作用变红色变红色变红色变红色变蓝色变蓝色不变色不变色倍速课时学练倍速课时学练倍速课时学练几种常见的酸实验10—2(1)观察盐酸、硫酸的颜色和状态(2)分别打开盛有盐酸、硫酸的试剂瓶的瓶盖,观察现象并闻气味
浓盐酸浓硫酸颜色、状态打开瓶盖后的现象气味无色液体无色粘稠液体在空气中会形成白雾无明显变化有刺激性气味无气味倍速课时学练倍速课时学练倍速课时学练二、浓盐酸的性质:挥发性:在空气中形成白雾无色液体,有刺激性气味思考:浓盐酸需要密封保存吗
思考:将浓盐酸放置在空气中,溶液质量会怎样变化
溶液的溶质的质量分数有什么变化
浓盐酸用途:重要的化工产品倍速课时学练倍速课时学练倍速课时学练2
浓硫酸的腐蚀性实验放置一会儿后的现象用玻璃棒蘸浓硫酸在纸上写字用小木棍蘸少量浓硫酸把浓硫酸滴到一小块布上由白色变成黑色变黑会穿洞,并变成黑色三、浓硫酸的性质:1、颜色状态气味密度无色无味粘稠液体倍速课时学练倍速课时学练倍速课时学练浓硫酸的腐蚀性——脱水作用能夺取纸张、木材、布料、皮肤里的水分,生成黑色的碳思考:浓硫酸把木材变黑是什么作用
这个变化是物理变化还是化学变化3、浓硫酸的吸水性浓硫酸可以吸收水(包括水蒸气),所以可以作为气体干燥剂思考:浓硫酸需要密封保存吗
思考:将浓硫酸放置在空气中,溶