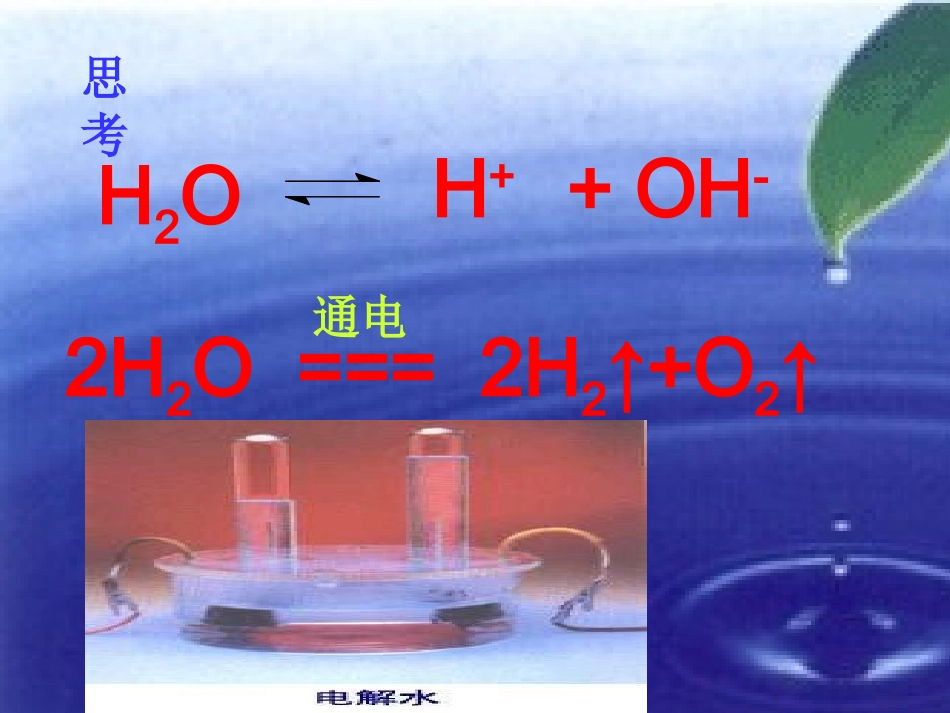
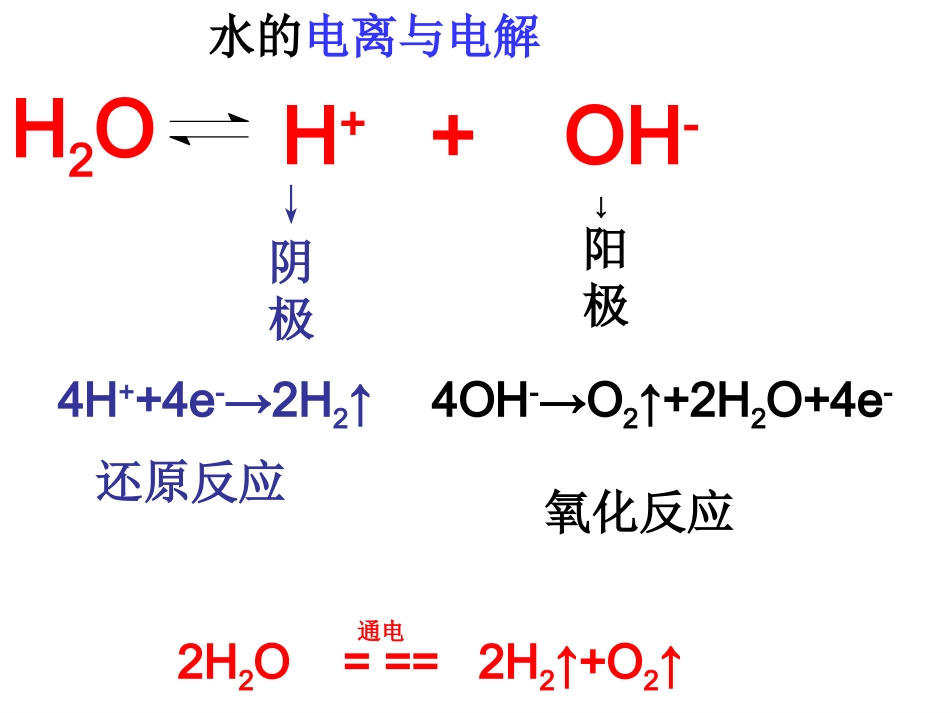
+-阴极阳极e-阳离子阴离子得电子还原反应失电子氧化反应e-H2OH++OH-2H2O===2H2↑+O2↑通电思考↓阴极↓阳极4OH-→O2↑+2H2O+4e-氧化反应4H++4e-→2H2↑还原反应2H2O===2H2↑+O2↑通电水的电离与电解H2OH++OH-1
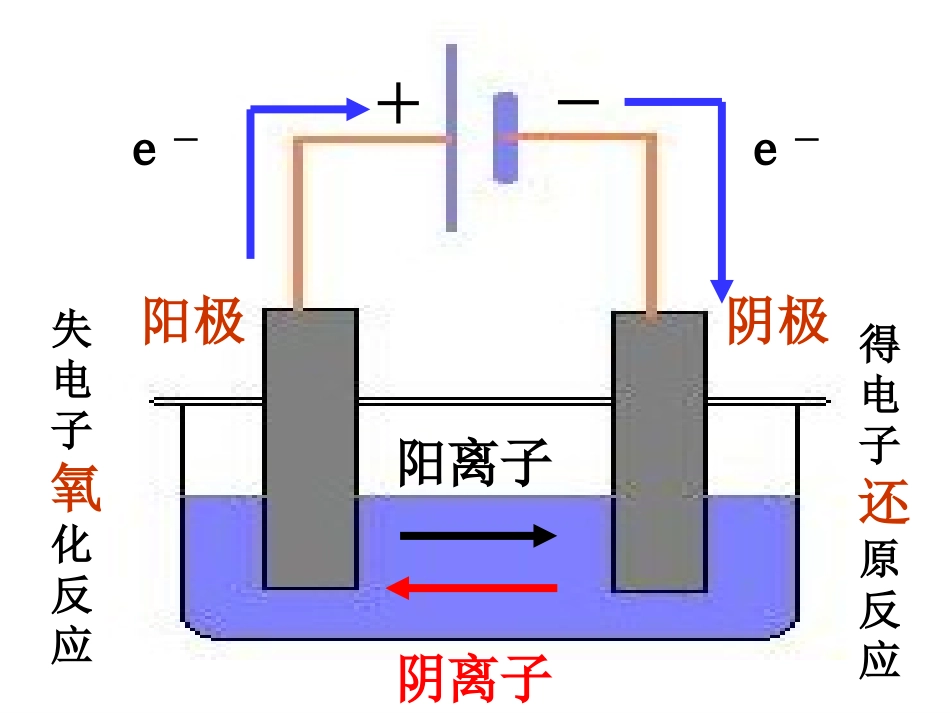
电解质溶液中,存在哪些离子
接通电源后,电子是如何流动的
接通电源后,溶液中各离子向哪个方向移动
4、移到两极表面将发生什么变化
5、在溶液中加入酚酞,然后通电,你将看到什么现象
饱和氯化钠溶液NaCl=Na++Cl-H2OH++OH-阴极阳极2Cl-→Cl2↑+2e-氧化反应2H++2e-→H2↑还原反应电源负极相连------电源正极相连电解过程通电后2NaCl+2H2O==2NaOH+H2↑+Cl2↑通电阴极产物阳极产物阳极2Cl-→Cl2↑+2e-阴极2H++2e-→H2↑2Cl-+2H2O==2OH-+H2↑+Cl2↑通电阳离子的氧化性强弱顺序5
离子的放电顺序K+Ca2+Na+Mg2+Al3+Zn2+Fe2+(H+)Cu2+Hg2+Ag+放电由难到易(得电子)[同浓度]阴离子还原性强弱顺序NO3-、OH-、Cl-、Br-、I-、S2-放电由难到易(失电子)Fe3+分析电解反应的一般思路:明确溶液中存在哪些离子根据阳极氧化,阴极还原分析得出产物阴阳两极附近有哪些离子阴极有红色金属析出阳极有气体析出该气体能使湿润的KI淀粉试纸变蓝阴极:Cu2++2e===Cu(还原反应)阳极:2Cl——2e==Cl2(氧化反应)阳极阴极CuCl2溶液+—C阴极:Cu2++2e===Cu(还原反应)阳极:2Cl——2e==Cl2(氧化反应)阴极阳极CuCl2溶液+—[阳极]:溶液中的阴离子向该极运动Cl-、OH-[阴极]:溶液中的阳离子向该极运动Cu2+、H+还原性Cl->OH-氧化性Cu2+>H+CuCl2