1专题11氯及其化合物【复习目标】1
了解氯单质及其重要化合物的主要性质及应用
了解氯单质及其重要化合物对环境质量的影响
掌握氯气的实验室制法包括所用试剂、仪器,反应原理和收集方法
【考情分析】高考对氯及其化合物考查常规实验、基本理论及化学计算相结合考查氯及其化合物的氧化性、特性及用途
近五年高考新课标卷共考查6次,题型主要为选择题和实验题出现,试题难度一般较大
【考点过关】考点一氯气的性质1
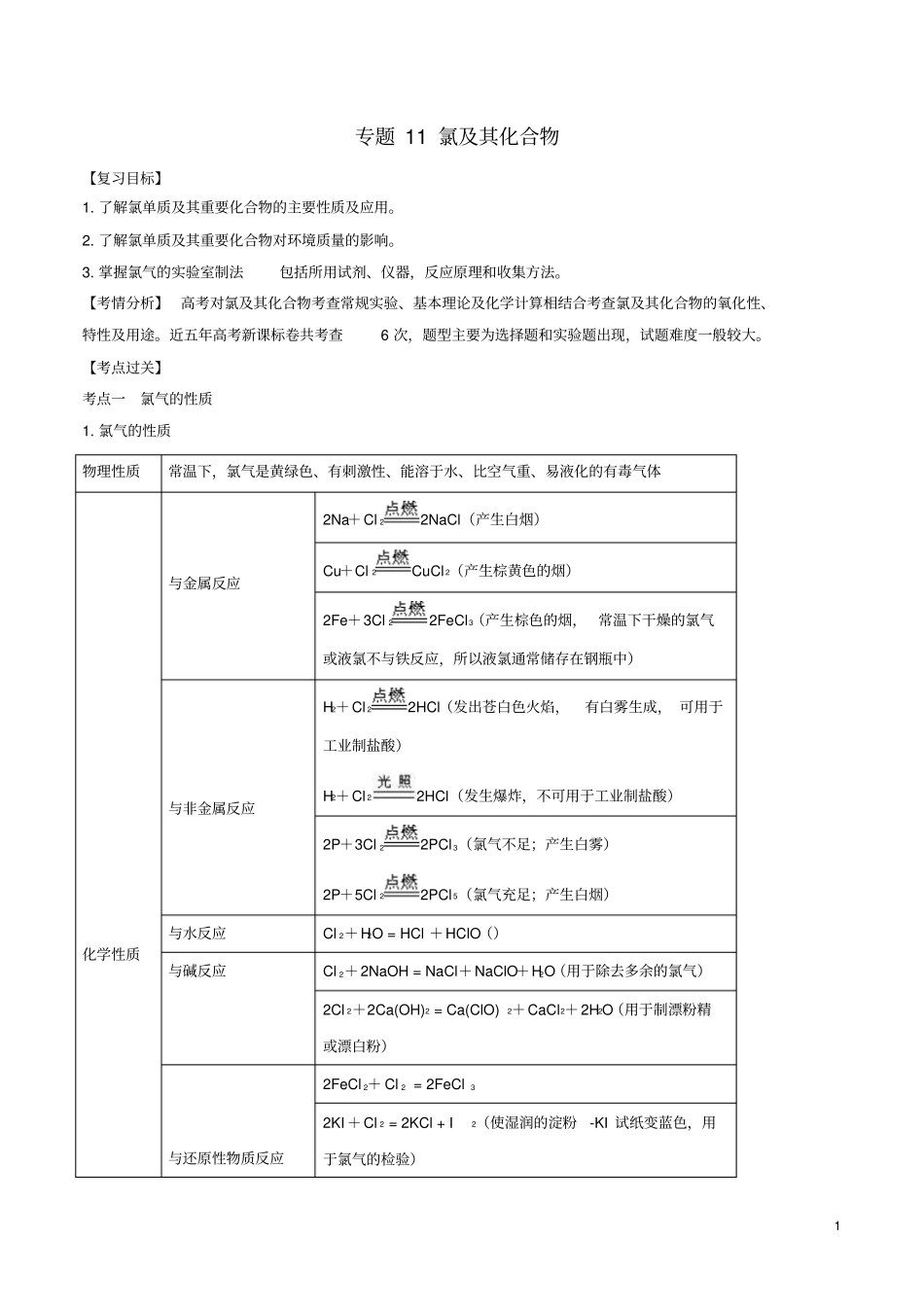
氯气的性质物理性质常温下,氯气是黄绿色、有刺激性、能溶于水、比空气重、易液化的有毒气体化学性质与金属反应2Na+Cl22NaCl(产生白烟)Cu+Cl2CuCl2(产生棕黄色的烟)2Fe+3Cl22FeCl3(产生棕色的烟,常温下干燥的氯气或液氯不与铁反应,所以液氯通常储存在钢瓶中)与非金属反应H2+Cl22HCl(发出苍白色火焰,有白雾生成,可用于工业制盐酸)H2+Cl22HCl(发生爆炸,不可用于工业制盐酸)2P+3Cl22PCl3(氯气不足;产生白雾)2P+5Cl22PCl5(氯气充足;产生白烟)与水反应Cl2+H2O=HCl+HClO()与碱反应Cl2+2NaOH=NaCl+NaClO+H2O(用于除去多余的氯气)2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O(用于制漂粉精或漂白粉)与还原性物质反应2FeCl2+Cl2=2FeCl32KI+Cl2=2KCl+I2(使湿润的淀粉-KI试纸变蓝色,用于氯气的检验)2SO2+Cl2+2H2O=2HCl+H2SO4(将SO2气体和Cl2气体混合后作用于有色溶液,漂白效果将大大减弱)与某些有机物反应CH4+Cl2CH3Cl+HCl(取代反应)CH2=CH2+Cl2→CH2ClCH2Cl(加成反应)2
氯水的组成与性质平衡关系Cl2+H2OHCl+HClO(部分反应)HClOH++ClO-(少量电离)H2OH+