1晶体结构与性质一、晶体常识1.晶体与非晶体晶体非晶体结构特征结构微粒周期性有序排列结构微粒无序排列性质特征自范性有无熔点固定不固定异同表现各向异性各向同性二者区别方法间接方法看是否有固定的熔点科学方法对固体进行X-射线衍射实验2
得到晶体的途径(1)熔融态物质凝固
(2)气态物质冷却不经液态直接凝固(凝华)
(3)溶质从溶液中析出
3.晶胞⑴概念:描述晶体结构的基本单元
(2)晶体中晶胞的排列——无隙并置①无隙:相邻晶胞之间没有任何间隙
②并置:所有晶胞平行排列、取向相同
与晶体有关的计算晶体结构的计算常常涉及如下数据:晶体密度、N、M、晶体体积、微粒间距离、微粒半径、夹角等,密A度的表达式往往是列等式的依据
解答这类题时,一要掌握晶体“均摊法”的原理,二要有扎实的立体几何知识,三要熟悉常见晶体的结构特征,并能融会贯通,举一反三
(1)“均摊法”原理2晶胞中任意位置上的一个原子如果被n个晶胞所共有,则每个晶胞对这个原子分得的份额就是1
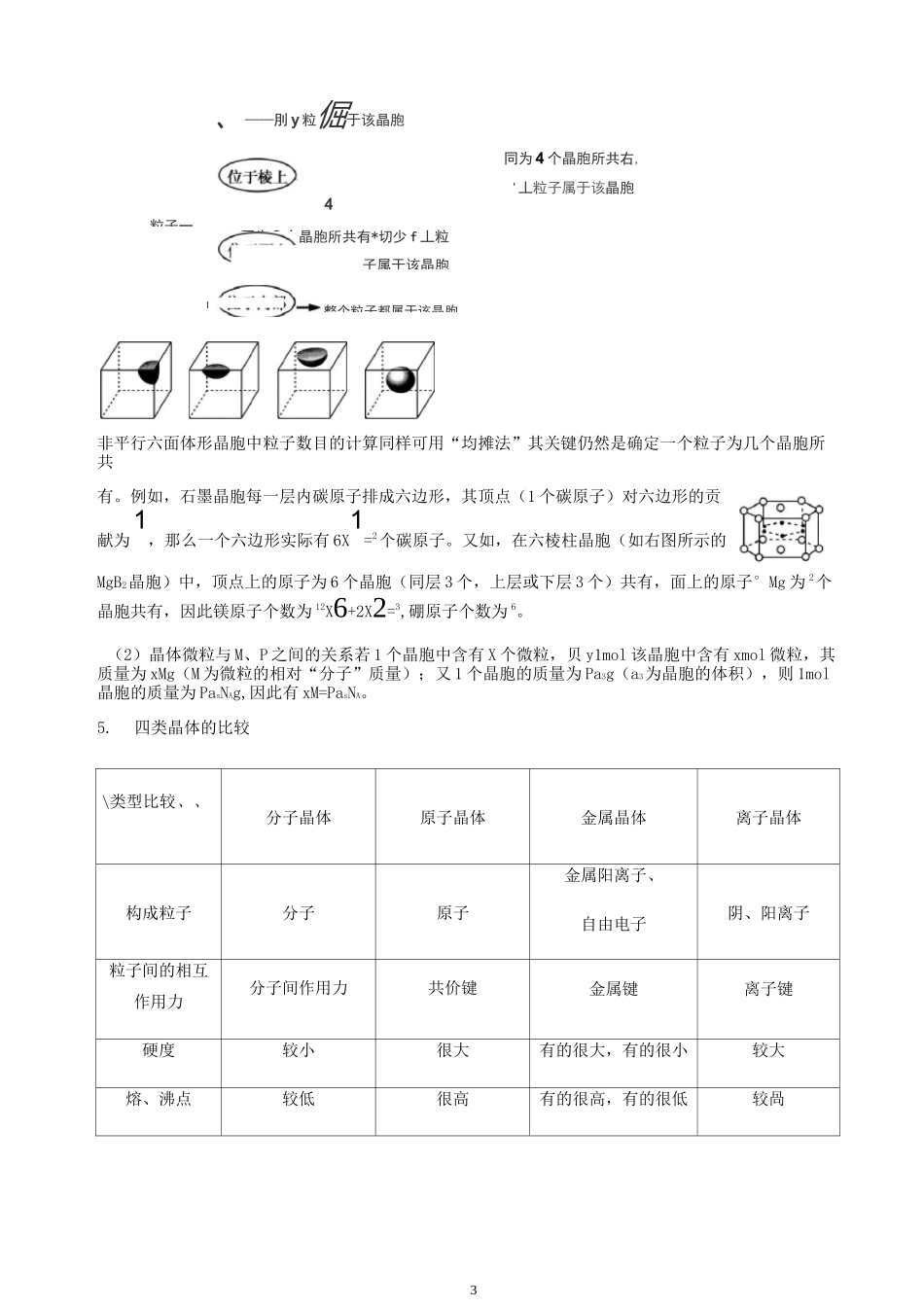
n3粒子一同为2个晶胞所共有*切少f丄粒子属于该晶胞」(位丁内、——刖y粒倔于该晶胞同为4个晶胞所共右,'丄粒子属于该晶胞4非平行六面体形晶胞中粒子数目的计算同样可用“均摊法”其关键仍然是确定一个粒子为几个晶胞所共有
例如,石墨晶胞每一层内碳原子排成六边形,其顶点(1个碳原子)对六边形的贡献为1,那么一个六边形实际有6X1=2个碳原子
又如,在六棱柱晶胞(如右图所示的MgB2晶胞)中,顶点上的原子为6个晶胞(同层3个,上层或下层3个)共有,面上的原子°Mg为2个晶胞共有,因此镁原子个数为12X6+2X2=3,硼原子个数为6
(2)晶体微粒与M、P之间的关系若1个晶胞中含有X个微粒,贝y1mol该晶胞中含有xmol微粒,其质量为xMg(M为微粒的相对“分子”质量);又1个晶胞的质量为Pa3g(a3为晶胞的体积),则1mol晶胞的