第3课时铝与氢氧化钠溶液的反应[学习目标定位]1
知道Al与NaOH溶液反应的产物及本质,能正确书写化学方程式和离子方程式
学会化学方程式计算的一般方法和步骤
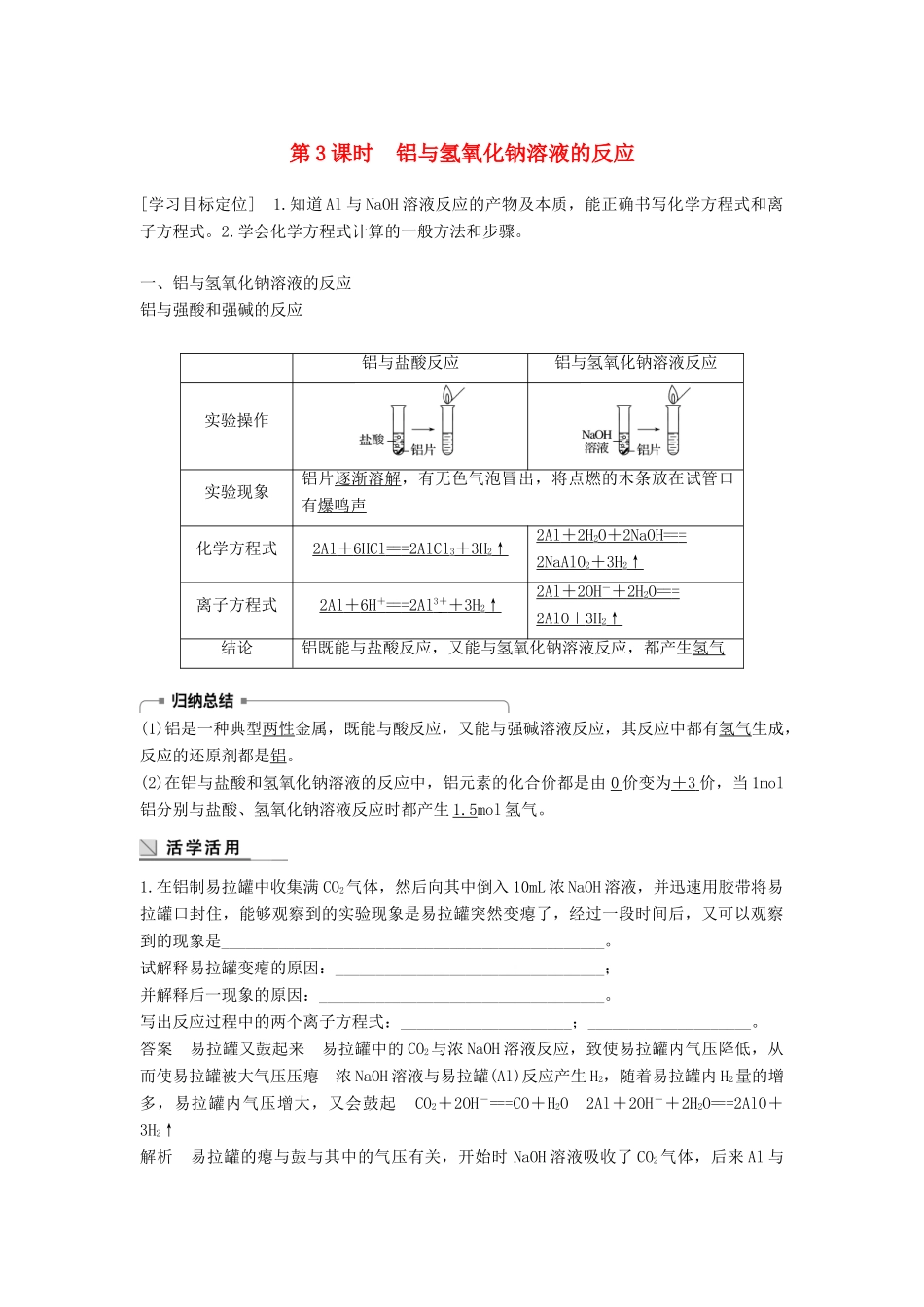
一、铝与氢氧化钠溶液的反应铝与强酸和强碱的反应铝与盐酸反应铝与氢氧化钠溶液反应实验操作实验现象铝片逐渐溶解,有无色气泡冒出,将点燃的木条放在试管口有爆鸣声化学方程式2Al+6HCl===2AlCl3+3H2↑2Al+2H2O+2NaOH===2NaAlO2+3H2↑离子方程式2Al+6H+===2Al3++3H2↑2Al+2OH-+2H2O===2AlO+3H2↑结论铝既能与盐酸反应,又能与氢氧化钠溶液反应,都产生氢气(1)铝是一种典型两性金属,既能与酸反应,又能与强碱溶液反应,其反应中都有氢气生成,反应的还原剂都是铝
(2)在铝与盐酸和氢氧化钠溶液的反应中,铝元素的化合价都是由0价变为+3价,当1mol铝分别与盐酸、氢氧化钠溶液反应时都产生1
5mol氢气
在铝制易拉罐中收集满CO2气体,然后向其中倒入10mL浓NaOH溶液,并迅速用胶带将易拉罐口封住,能够观察到的实验现象是易拉罐突然变瘪了,经过一段时间后,又可以观察到的现象是_______________________________________________
试解释易拉罐变瘪的原因:_________________________________;并解释后一现象的原因:___________________________________
写出反应过程中的两个离子方程式:_____________________;____________________
答案易拉罐又鼓起来易拉罐中的CO2与浓NaOH溶液反应,致使易拉罐内气压降低,从而使易拉罐被大气压压瘪浓NaOH溶液与易拉罐(Al)反应产生H2,随着易拉罐内H2量的增多,易拉罐内气压增大,