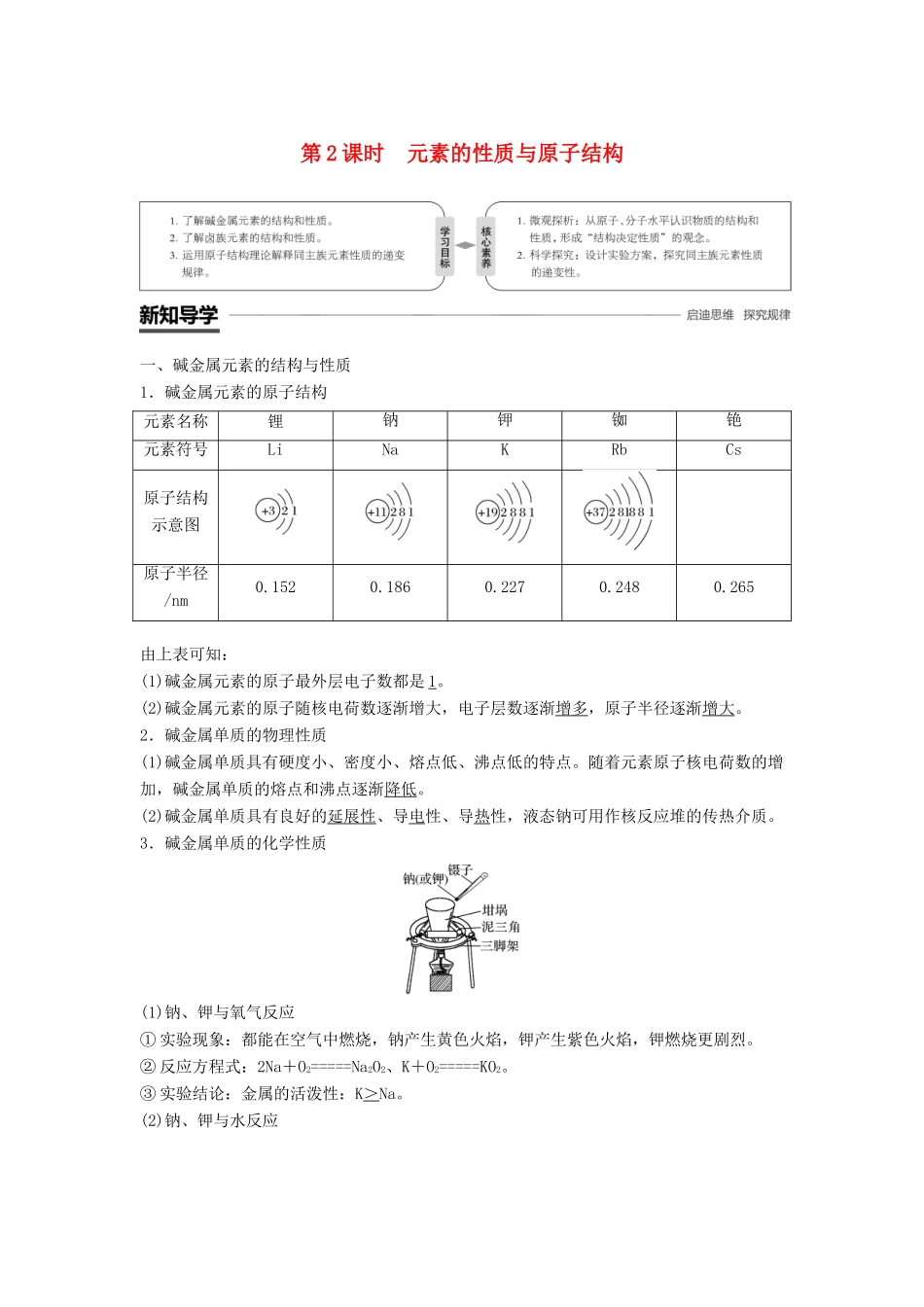
第2课时元素的性质与原子结构一、碱金属元素的结构与性质1.碱金属元素的原子结构元素名称锂钠钾铷铯元素符号LiNaKRbCs原子结构示意图原子半径/nm0
265由上表可知:(1)碱金属元素的原子最外层电子数都是1
(2)碱金属元素的原子随核电荷数逐渐增大,电子层数逐渐增多,原子半径逐渐增大
2.碱金属单质的物理性质(1)碱金属单质具有硬度小、密度小、熔点低、沸点低的特点
随着元素原子核电荷数的增加,碱金属单质的熔点和沸点逐渐降低
(2)碱金属单质具有良好的延展性、导电性、导热性,液态钠可用作核反应堆的传热介质
3.碱金属单质的化学性质(1)钠、钾与氧气反应①实验现象:都能在空气中燃烧,钠产生黄色火焰,钾产生紫色火焰,钾燃烧更剧烈
②反应方程式:2Na+O2=====Na2O2、K+O2=====KO2
③实验结论:金属的活泼性:K>Na
(2)钠、钾与水反应①实验现象:相同点:金属浮在水面上;熔成闪亮的小球;小球四处游动;发出嘶嘶的响声;反应后的溶液呈红色
不同点:钾与水的反应有轻微爆炸声并着火燃烧
②化学方程式:2Na+2H2O===2NaOH+H2↑;2K+2H2O===2KOH+H2↑
③实验结论:与水反应剧烈程度:K>Na;金属的活泼性:K>Na
(1)碱金属的原子结构与化学性质的递变关系从Li到Cs,随核电荷数的增加,电子层数逐渐增多,原子半径逐渐增大,原子核对最外层电子的引力逐渐减弱,元素金属性逐渐增强;单质的还原性逐渐增强,离子的氧化性逐渐减弱
(2)碱金属的化学性质及比较LiNaKRbCs单质与氧气反应越来越剧烈,产物分别是Li2ONa2O、Na2O2K2O、K2O2、KO2更复杂氧化物与水反应越来越剧烈,现象分别是反应缓慢剧烈反应轻微爆炸剧烈爆炸化合物碱性强弱:LiOH<NaOH<KOH<RbOH<CsOH例1下列有