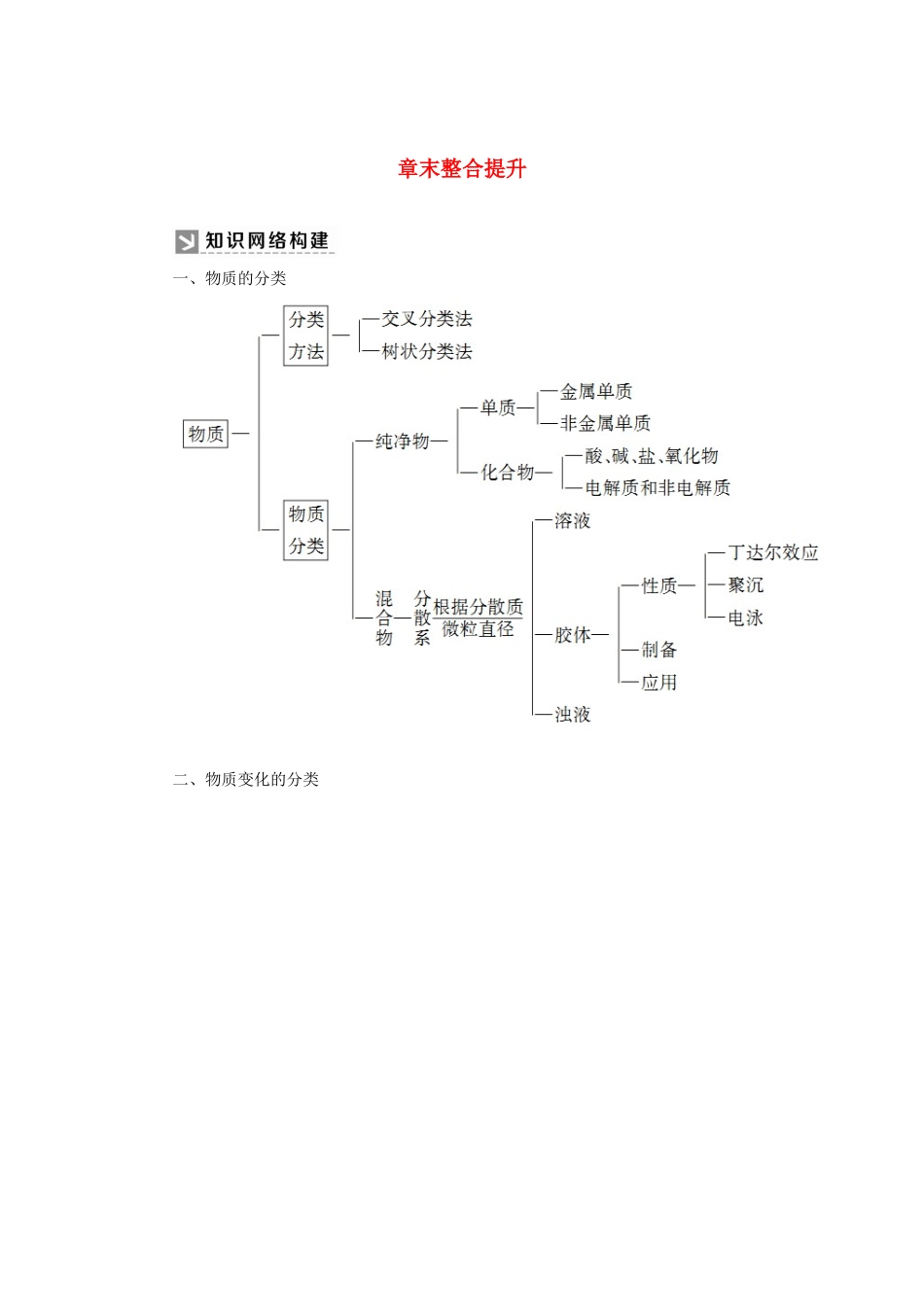
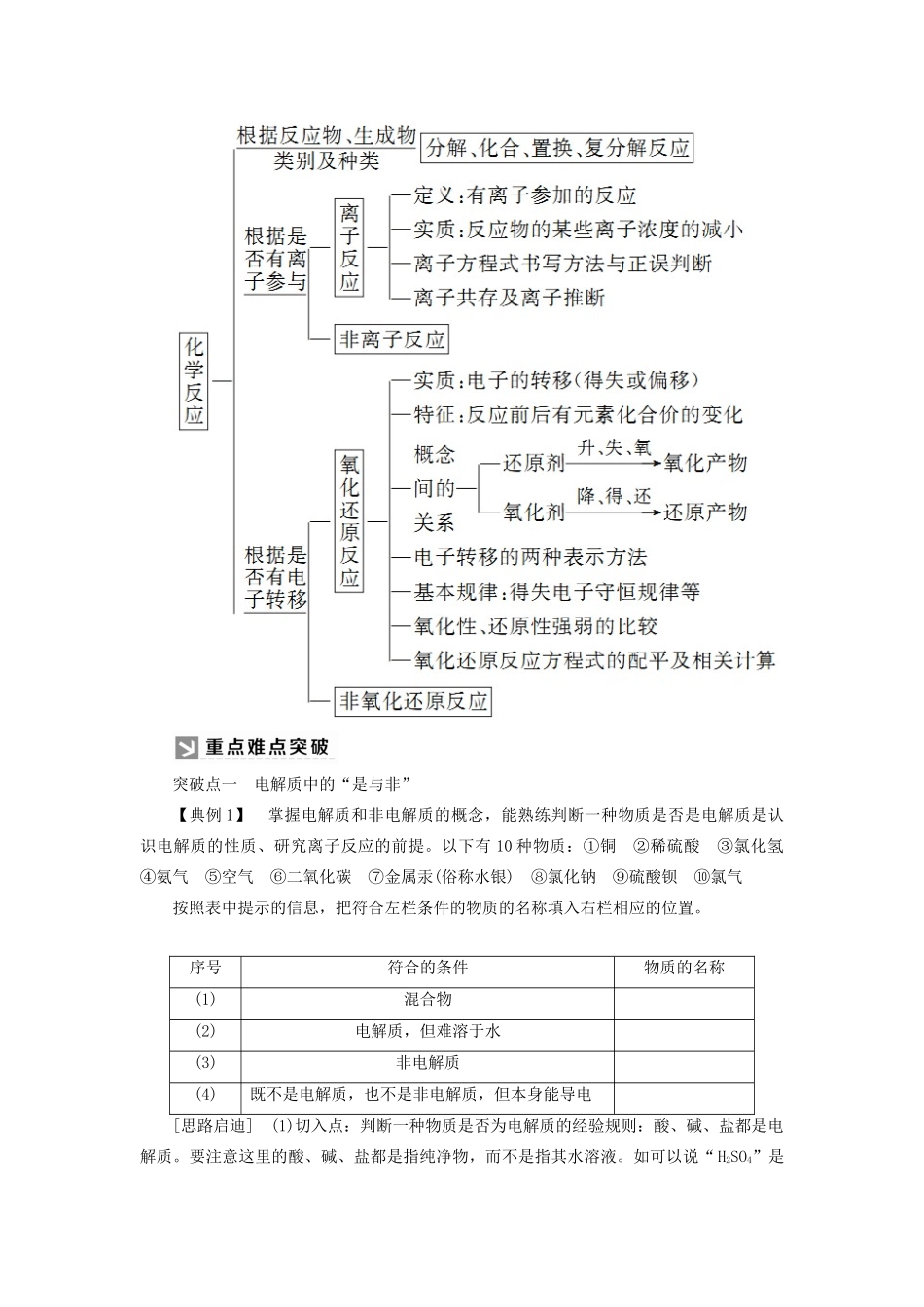
章末整合提升一、物质的分类二、物质变化的分类突破点一电解质中的“是与非”【典例1】掌握电解质和非电解质的概念,能熟练判断一种物质是否是电解质是认识电解质的性质、研究离子反应的前提
以下有10种物质:①铜②稀硫酸③氯化氢④氨气⑤空气⑥二氧化碳⑦金属汞(俗称水银)⑧氯化钠⑨硫酸钡⑩氯气按照表中提示的信息,把符合左栏条件的物质的名称填入右栏相应的位置
序号符合的条件物质的名称(1)混合物(2)电解质,但难溶于水(3)非电解质(4)既不是电解质,也不是非电解质,但本身能导电[思路启迪](1)切入点:判断一种物质是否为电解质的经验规则:酸、碱、盐都是电解质
要注意这里的酸、碱、盐都是指纯净物,而不是指其水溶液
如可以说“H2SO4”是电解质,但不能说“稀硫酸”是电解质
(2)关键点:①物质范畴:化合物
②导电条件:水溶液或熔融状态
③导电本质:自身发生电离
[解析]10种物质中稀硫酸和空气属于混合物
BaSO4是难溶性电解质
而NH3、CO2的水溶液虽然能导电,但不是它们本身发生了电离,而是它们与水发生了反应,生成了电解质NH3·H2O和H2CO3,故它们属于非电解质
铜和金属汞属于单质,不是化合物,故既不是电解质也不是非电解质,但能导电;稀硫酸是混合物,既不是电解质也不是非电解质,但能导电
[答案](1)稀硫酸、空气(2)硫酸钡(3)氨气、二氧化碳(4)铜、金属汞、稀硫酸(1)电解质、非电解质的相同之处在于它们都是化合物,单质和混合物既不属于电解质,又不属于非电解质;电解质、非电解质的不同之处是在水溶液里或熔融状态下能否导电
(2)电解质概念中的“或”,指两种情况满足一种即可;非电解质中的“无论”和“都”,指两种情况必须同时满足
(3)从物质类别上把握概念更清晰明了
如:酸、碱、金属氧化物、大多数盐以及H2O为电解质
酒精、蔗糖和大多数非金属氧化物是非电解质
(4)能导电的物质不一