第2章海水中的重要元素——钠和氯一、海水中的重要元素——钠和氯二、“化合价—物质类别”二维图1.钠及其化合物的“价—类二维图”①4Na+O2===2Na2O②2Na+O2=====Na2O2③2Na+2H2O===2NaOH+H2↑④Na2O+H2O===2NaOH⑤2Na2O2+2H2O===4NaOH+O2↑⑥NaOH+HCl===NaCl+H2O⑦Na2O+2HCl===2NaCl+H2O⑧2Na+Cl2=====2NaCl⑨2NaCl(熔融)=====2Na+Cl2↑2.氯及其化合物的“价——类二维图”①H2+Cl2=====2HCl②Cl2+H2O===HCl+HClO③Cl2+2NaOH===NaCl+NaClO+H2O④2HCl=====H2↑+Cl2↑⑤HCl+KOH===KCl+H2O⑥NaClO+CO2+H2O===HClO+NaHCO3⑦NaClO+2HCl===NaCl+Cl2↑+H2O⑧2KClO3+SO2===2ClO2+K2SO4(拓展反应)⑨Cl2O7+H2O===2HClO4⑩NaOH+HClO4===NaClO4+H2O⑪2ClO2+H2O2+2NaOH===2NaClO2+2H2O+O2↑[项目探究]过氧化钠与CO2反应原理的实验探究[实验情境]实验1:用脱脂棉包住一些Na2O2粉末放在石棉网上,向脱脂棉上滴几滴水,一会脱脂棉剧烈燃烧
实验2:用脱脂棉包住一些Na2O2粉末放在石棉网上,用干净消毒的玻璃管插入脱脂棉中吹气,一会脱脂棉剧烈燃烧
上述实验1可以说明Na2O2与H2O反应放出O2同时放热,那么实验2可以说明Na2O2与CO2反应放出O2同时放热吗
[实验目的]探究Na2O2与CO2反应的条件及反应原理
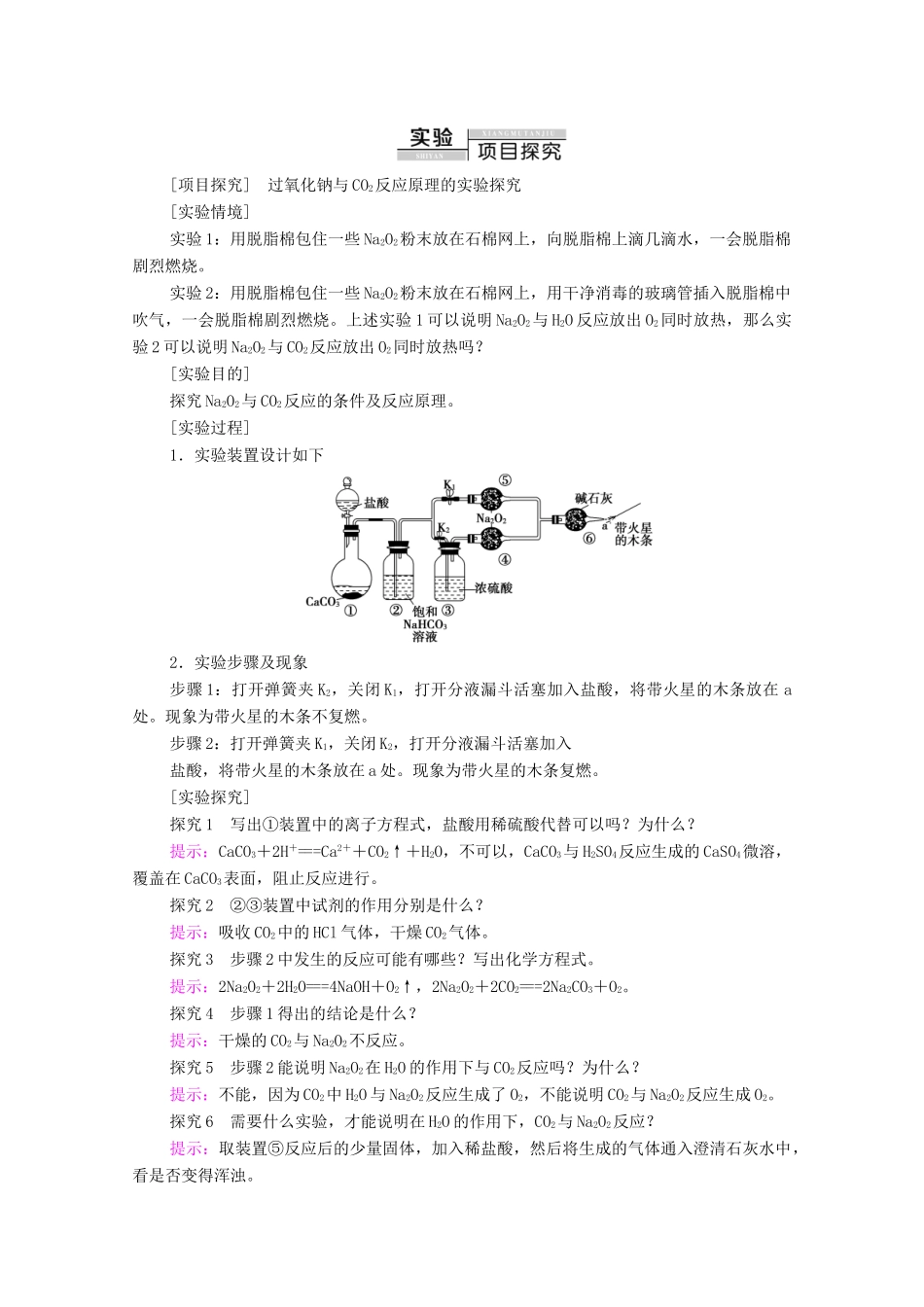
[实验过程]1.实验装置设计如下2.实验步骤及现象步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放