卤族元素1.了解卤族元素在周期表中的位置
2.了解卤素原子的结构特点
3.了解卤素单质的物理性质和化学性质
4.揭示结构与性质的内在联系
1.卤素单质的物理性质的相似性和递变性
单质F2→Cl2→Br2→I2相似性颜色都有颜色毒性都有毒递变性状态从气态到固态颜色逐渐加深密度逐渐增大熔、沸点逐渐升高2
卤素单质的化学性质的相似性和递变性
(1)卤素单质与氢气的反应
单质F2Cl2Br2I2相似性H2+X2===2HX(X代表卤素原子)递变性反应条件黑暗光照或点燃加热不断加热反应剧烈程度越来越弱产物的稳定性HF>HCl>HBr>HI(2)卤素单质间的置换反应
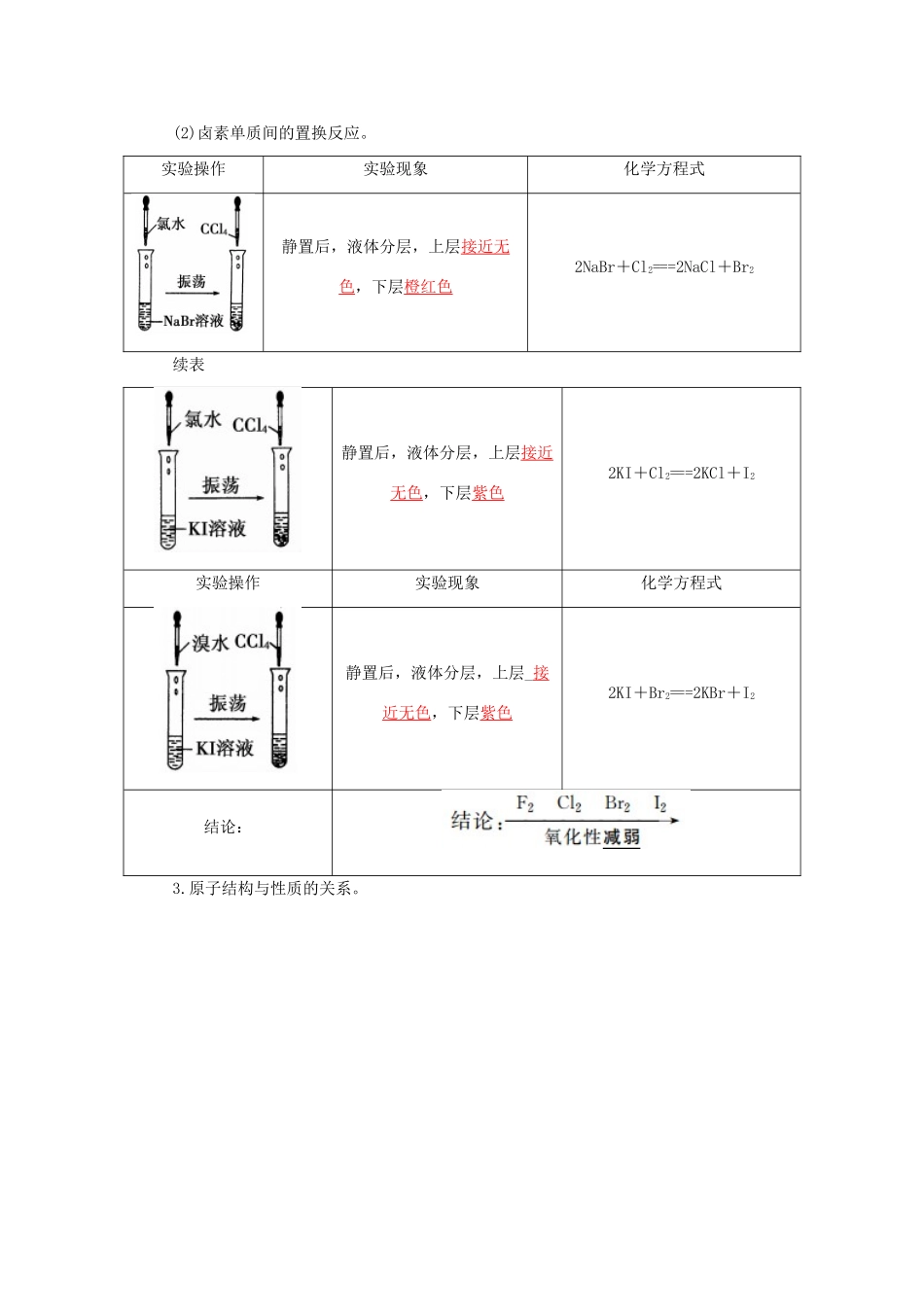
实验操作实验现象化学方程式静置后,液体分层,上层接近无色,下层橙红色2NaBr+Cl2===2NaCl+Br2续表静置后,液体分层,上层接近无色,下层紫色2KI+Cl2===2KCl+I2实验操作实验现象化学方程式静置后,液体分层,上层_接近无色,下层紫色2KI+Br2===2KBr+I2结论:3
原子结构与性质的关系
【应用思考】1.结合同主族元素性质的递变规律,判断H3PO4和H3AsO4酸性的强弱;H2O和H2S的稳定性
提示:同主族元素,原子序数越大,非金属性越弱,其最高价含氧酸酸性越弱,气态氢化物稳定性越弱
故酸性:H3PO4>H3AsO4,稳定性:H2O>H2S
2.请写出两个离子反应以证明氧化性强弱为:Cl2>Br2>I2
提示:Cl2+2Br-===Br2+2Cl-,Br2+2I-===I2+2Br-
1.关于卤素(用X表示)的下列叙述正确的是(C)A.卤素单质与水反应均可用X2+H2O===HXO+HX表示B.HX热稳定性随核电荷数增加而增强C.卤素单质的颜色从F2→I2随相对分子质量增大而逐渐加深D.X-离子的还原性依次为:F-<Cl-<Br-<I-,因此相对分子质量小的卤素单质可将相对分子质量大的卤素