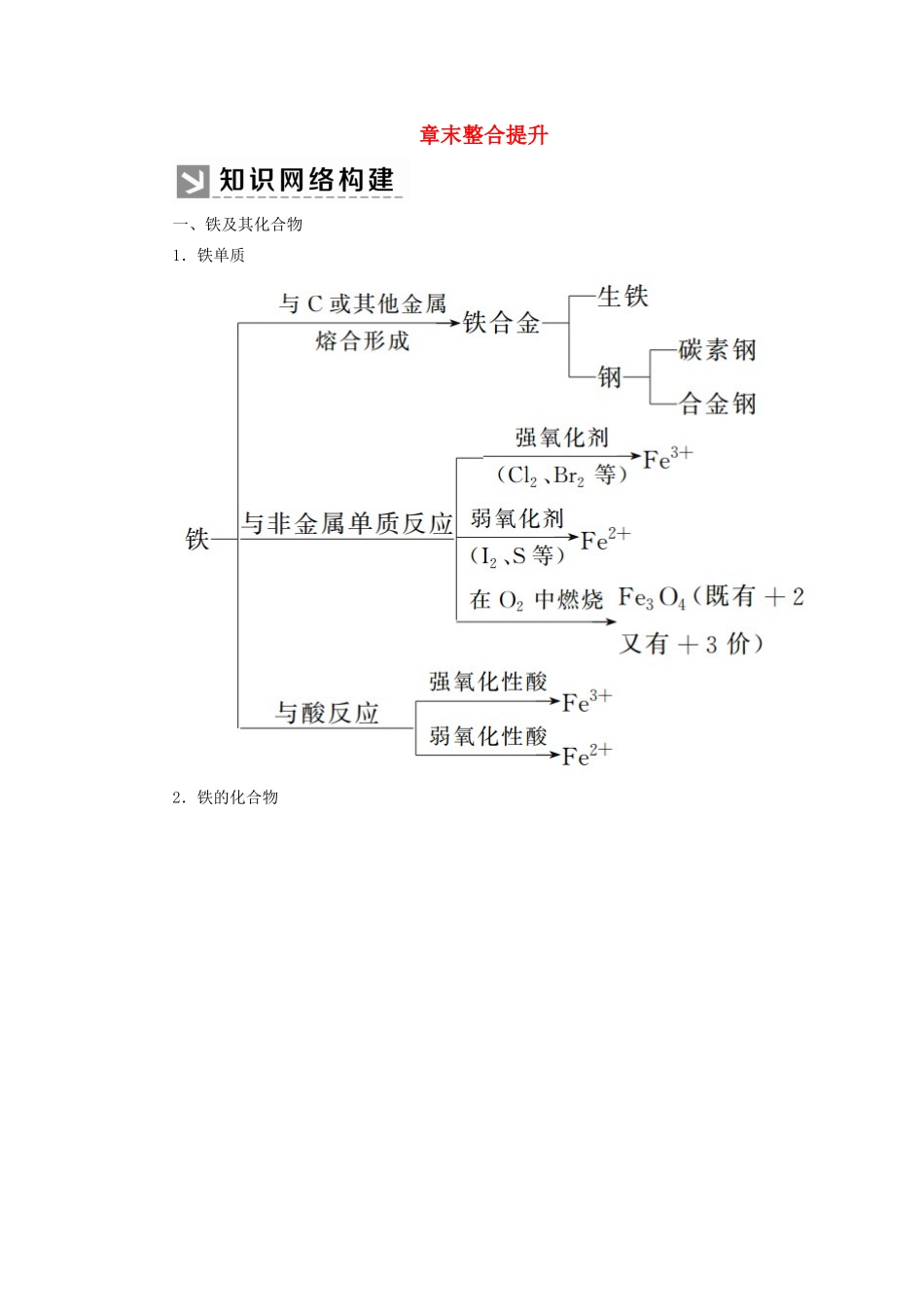
章末整合提升一、铁及其化合物1.铁单质2.铁的化合物二、铝及铝合金突破点一Fe3+、Fe2+、Cu、Fe之间的转化【典例1】已知Cu+2Fe3+===Cu2++2Fe2+,Zn+2Fe3+===Zn2++2Fe2+,现把等物质的量的CuSO4、FeCl3和Zn三种物质置于盛有水的容器中,充分反应后,容器中除SO、Cl-外还有()A.Zn2+、Cu、Fe2+B.Zn2+、Cu2+、Fe、Fe2+C.Zn2+、Cu2+、Fe2+D.Zn2+、Cu2+、Cu、Fe2+[思路启迪](1)切入点:要考虑到一种金属与多种阳离子发生反应时,阳离子按氧化性由强到弱的顺序发生反应
按发生反应的先后排序,结合题中的“量”推算反应的最终产物
(2)关键点:正确分析反应的先后顺序
在同一溶液中,当发生氧化还原反应时,一定是氧化性最强的物质先与还原剂反应
另外在求解过程中还要考虑各反应物之间量的关系
[解析]设CuSO4、FeCl3和Zn的物质的量均为1mol,由题中所给的反应式可得出氧化性:Fe3+>Cu2+,所以Zn先与Fe3+反应,1molFe3+消耗0
5molZn;剩余的0
5molZn能置换出0
5molCu,溶液中还剩余0
5molCu2+,即充分反应后,容器中还含有Fe2+、Zn2+、Cu2+、Cu
[答案]D判断化学反应先后顺序的方法(1)一种氧化剂与多种还原剂反应,还原性强的还原剂优先发生反应
如向含等物质的量浓度的碘化亚铁、溴化亚铁溶液中缓慢通入氯气,发生反应的先后顺序为I-、Fe2+、Br-
(2)一种还原剂与多种氧化剂反应,氧化性强的氧化剂优先发生反应
如在含等物质的量浓度的H+、Fe2+、Fe3+、Cu2+、Zn2+的溶液中加入镁粉,反应的先后顺序为Fe3+、Cu2+、H+、Fe2+、Zn2+
(3)一种碱与多种阳离子反应,生成物越难电离,越先发生反应
如在含等物质的量浓