第六章化学能与热能[考纲解读]1
了解化学反应中能量转化的原因及常见的能量转化形式
了解化学能与热能的相互转化
了解吸热反应、放热反应、反应热等概念
了解热化学方程式的含义,能正确书写热化学方程式
了解能源是人类生存和社会发展的重要基础
了解化学在解决能源危机中的重要作用
了解焓变(ΔH)与反应热的含义
理解盖斯定律,能用盖斯定律进行有关反应焓变的计算
第19讲焓变热化学方程式一、焓变1.焓变和反应热(1)反应热:化学反应中□吸收或放出的热量
(2)焓变:生成物与反应物的内能差,ΔH=H(生成物)-H(反应物)
在恒压条件下化学反应的热效应,其符号为□ΔH,单位是□kJ·mol-1或kJ/mol
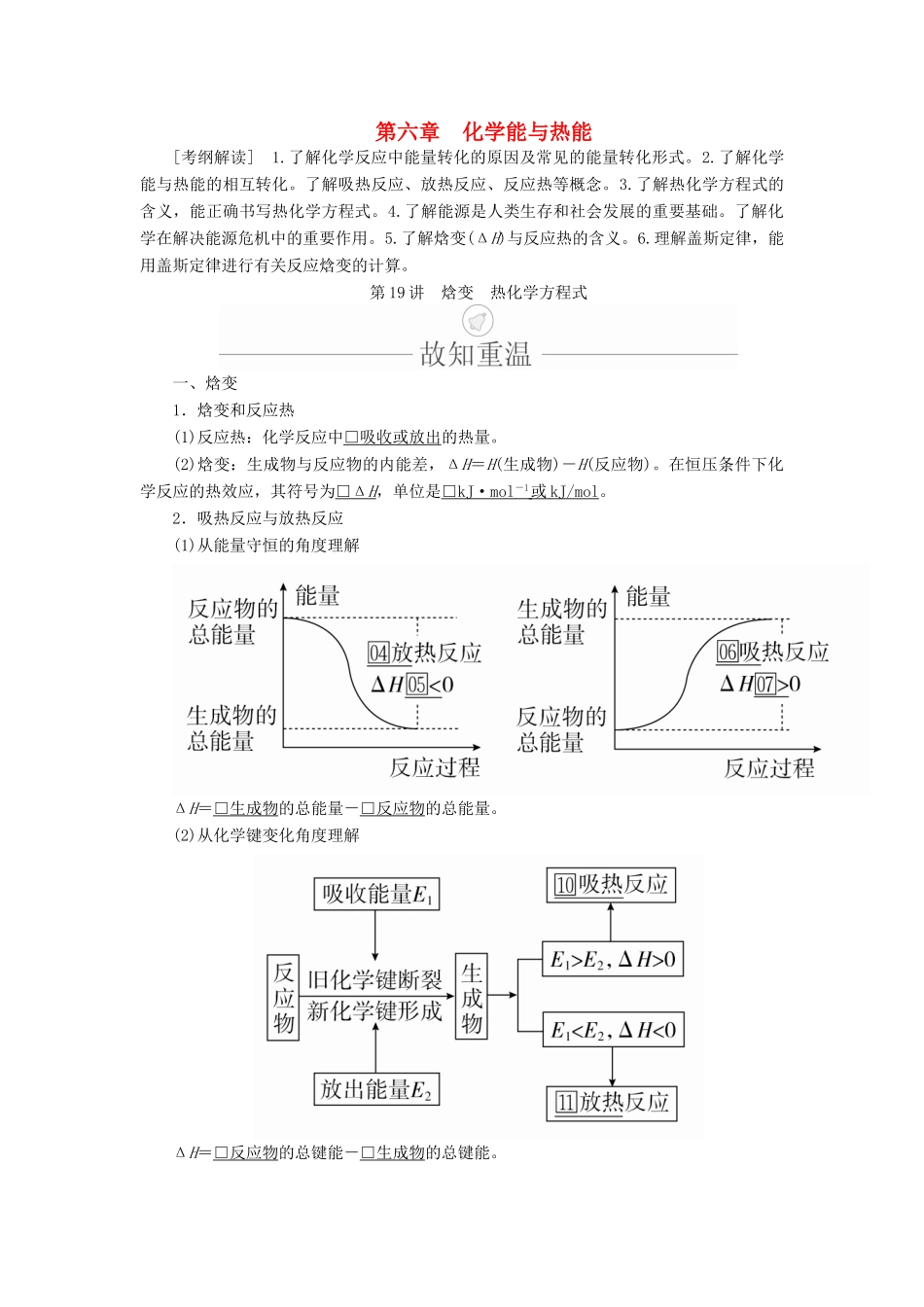
2.吸热反应与放热反应(1)从能量守恒的角度理解ΔH=□生成物的总能量-□反应物的总能量
(2)从化学键变化角度理解ΔH=□反应物的总键能-□生成物的总键能
(3)常见的放热反应和吸热反应①放热反应:大多数化合反应、□中和反应、金属与□酸的反应、所有的燃烧反应
②吸热反应:大多数分解反应、盐的□水解反应、Ba(OH)2·8H2O和NH4Cl反应、C与H2O(g)反应、C与CO2反应
二、热化学方程式1.概念:表示参加反应□物质的量和□反应热的关系的化学方程式
2.意义:不仅表明了化学反应中的物质变化,也表明了化学反应中的□能量变化
例如:H2(g)+O2(g)===H2O(l)ΔH=-285
8kJ·mol-1,表示在25℃和1
01×105Pa下,1mol氢气和0
5mol氧气完全反应生成1mol液态水时放出285
8kJ的热量
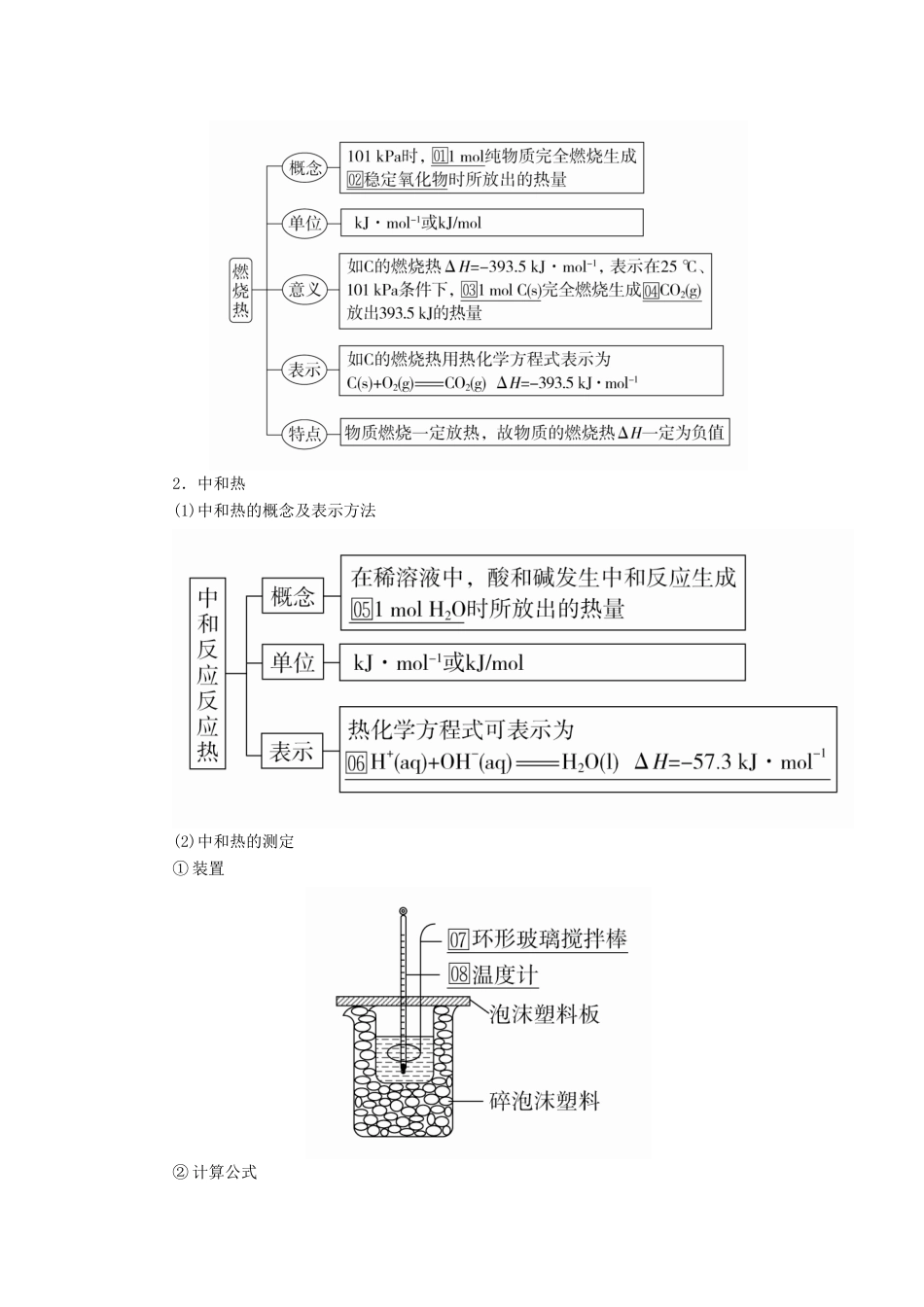
3.热化学方程式的书写三、燃烧热与中和热能源1.燃烧热2.中和热(1)中和热的概念及表示方法(2)中和热的测定①装置②计算公式ΔH=-kJ·mol-1t1——起始温度,t2——终止温度
(3)注意事项①泡沫塑料板和碎泡沫塑料(或纸条)