章末整合提升突破点一元素周期表和元素周期律【典例1】四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性
下列说法正确的是()A.简单离子半径:WI,则HCl,HBr,HI的热稳定性依次减弱,C项错误;电子层结构相同,则M的原子序数-1=R的原子序数+2,则原子序数为RY>XB.最高价氧化物对应水化物的酸性:X>W>ZC.最简单气态氢化物的热稳定性:Y>X>W>ZD.元素X、Z、W的最高化合价分别与其主族序数相等[思路启迪](1)切入点:根据周期表结构推断X、Y为第二周期元素,Z、W为第三周期元素,并根据已知条件确定W元素
(2)关键点:熟练掌握元素周期表中同周期、同主族性质的递变规律
[解析]根据题目中所给周期表短周期的一部分可知,X、Y是第二周期元素,Z、W为第三周期元素,又因为W质子数是最外层电子数的3倍,可推出W是P,根据位置关系,X、Y、Z分别为N、O、Si
A选项中,原子半径大小关系是:Si>P>N>O,故A错误
B选项,非金属性越强,最高价氧化物对应水化物的酸性越强,非金属性:O>N>P>Si,故B正确
C选项中,非金属性越强,简单氢化物的热稳定性越强,故C正确
D选项中,主族元素的最高正化合价等于主族序数(O、F除外),故D正确
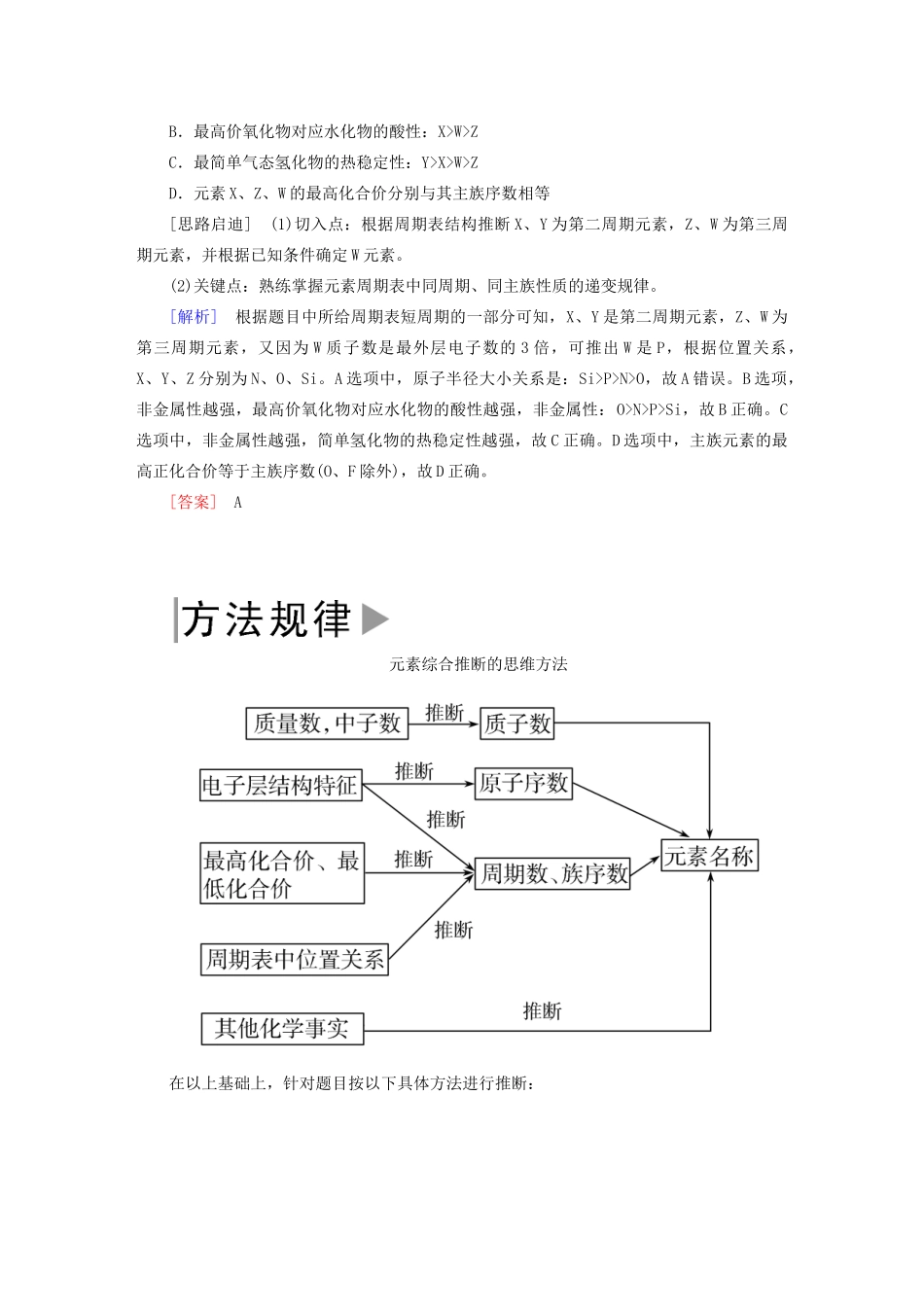
[答案]A元素综合推断的思维方法在以上基础上,针对题目按以下具体方法进行推断:[针对训练2]下表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素的核电荷数为X元素的2倍
下列说法正确的是()XYZWTA
X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次递增B.Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增C.YX2晶体熔化、液态WX3气化均需克服分子