第1课时酸、碱、盐在水溶液中的电离学习目标1
了解电解质、非电解质和电离的概念
会书写电离方程式
从电离的角度认识酸、碱、盐
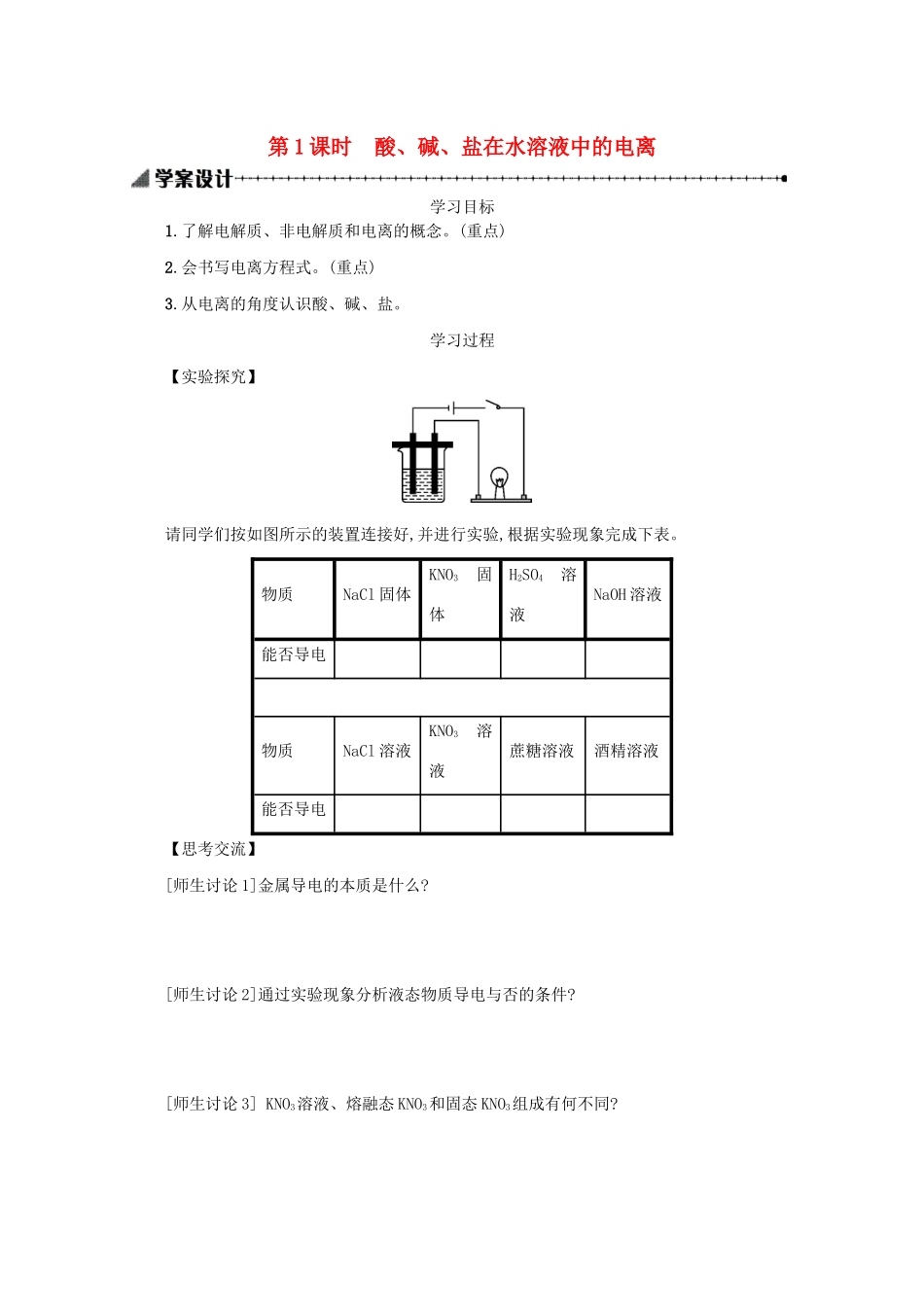
学习过程【实验探究】请同学们按如图所示的装置连接好,并进行实验,根据实验现象完成下表
物质NaCl固体KNO3固体H2SO4溶液NaOH溶液能否导电物质NaCl溶液KNO3溶液蔗糖溶液酒精溶液能否导电【思考交流】[师生讨论1]金属导电的本质是什么
[师生讨论2]通过实验现象分析液态物质导电与否的条件
[师生讨论3]KNO3溶液、熔融态KNO3和固态KNO3组成有何不同
一、电解质和非电解质的概念1
概念电解质:在状态下能导电的
非电解质:在状态下都不能导电的
SO2属于化合物,溶于水也能导电,SO2属于电解质吗
【练习1】下列物质哪些能导电
哪些是电解质
哪些是非电解质
(1)金属铜(2)碳棒(3)O2(4)H2SO4(5)液态HCl(6)CH3COOH(7)葡萄糖(8)固态NaCl(9)CaCO3固体(10)CuSO4·5H2O(11)熔融状态的KNO3(12)KOH水溶液(13)酒精水溶液(14)盐酸(15)CaO(16)CO2(17)H2O(18)NH3二、电离1
电离的表示——电离方程式(1)概念:
(2)书写步骤:三、从电离角度认识酸、碱、盐1
酸:电离时生成的阳离子全部都是氢离子的化合物
【练习2】书写下列物质的电离方程式:KCl、Na2SO4、AgNO3、BaCl2、NaHSO4、NaHCO3
【练习3】下面叙述正确的是()A
NaCl溶液能导电,所以NaCl溶液是电解质B
固态NaCl不导电,但NaCl是电解质C
HCl水溶液能导电,所以HCl是电解质D
SO3溶于水能导电,所以SO3是电解质E
Cu能导电,所以是电解质F
BaSO4的水溶液不能导电,所以BaSO4是非电解质