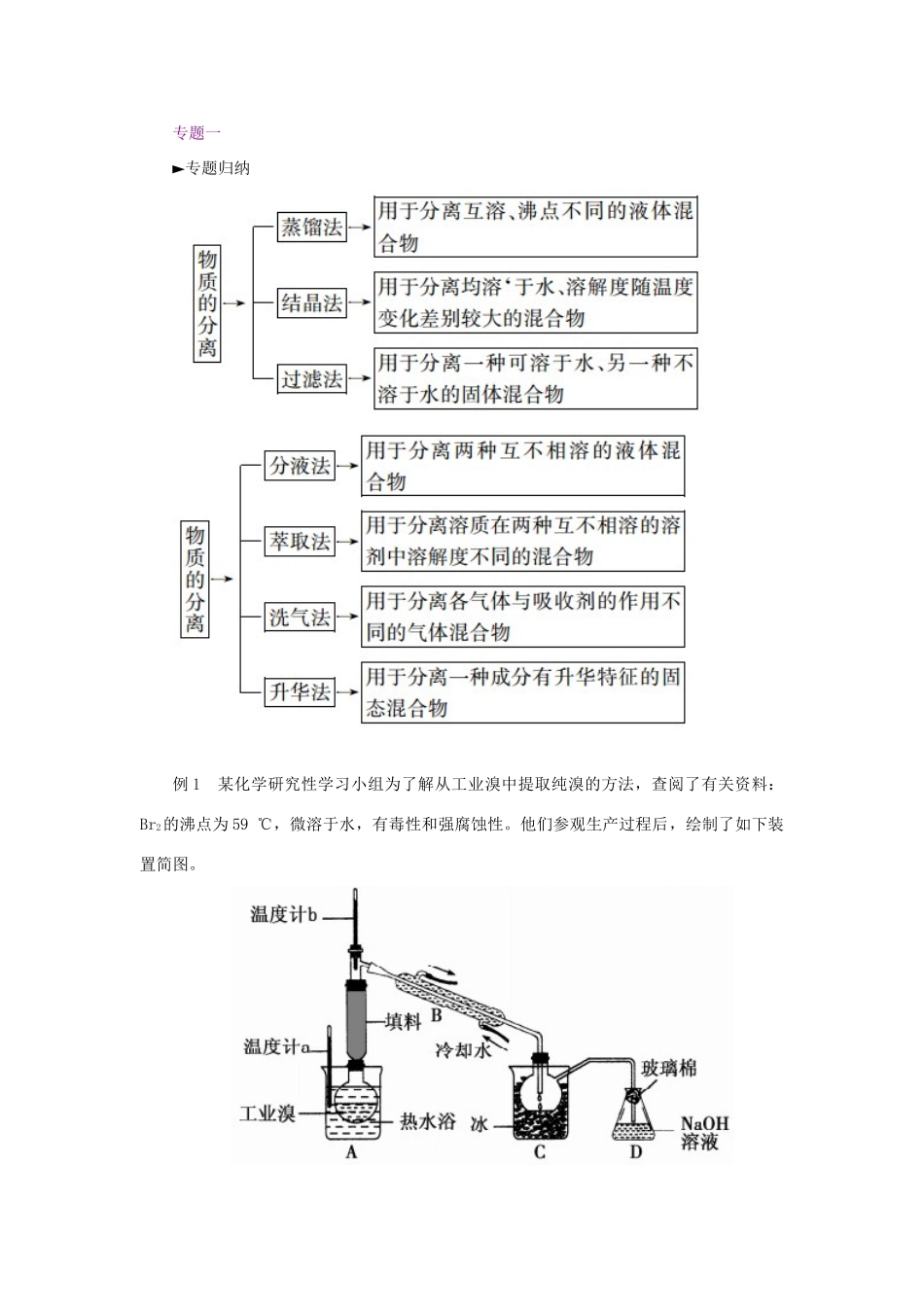
化学与自然资源的开发利用专题一►专题归纳例1某化学研究性学习小组为了解从工业溴中提取纯溴的方法,查阅了有关资料:Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性
他们参观生产过程后,绘制了如下装置简图
请你参与分析讨论
(1)图中仪器B的名称:____________
(2)整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因为_______________________________________________________
(3)实验装置气密性良好,要达到提取纯溴的目的,操作中如何控制关键条件:_____________________________________________
(4)C中液体产物颜色为____________,为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是____________
解析:由已知信息Br2有强腐蚀性可得出Br2腐蚀橡胶,故装置中不能用橡胶塞和橡胶管
再由Br2的沸点为59℃可知用该套装置提取纯溴关键要控制温度计b的温度,收集59℃时的馏分
C中收集到的是深红棕色的液溴,要除去该产物中残留的少量Cl2,可向其中加入NaBr充分反应后,利用Br2难溶于水的性质进行分液来分离,或利用Br2易挥发的特点用蒸馏法分离
答案:(1)冷凝管(2)Br2腐蚀橡胶(3)控制温度计b的温度,并收集59℃时的馏分(4)深红棕色分液(或蒸馏)►专题训练1.(1)在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大原因
经检测某工厂废液中含有大量的Mg2+、Al3+、Ag+、Fe3+、Ba2+
试分析回答下列问题
①该废液中可能大量存在的阴离子是__________
A.SOB.NOC.Cl-D.CO②为了充分利用资源和保护环境,今要回收废液中的金属银,请你设计一个回收实验方案,并写出有关离子反应方程