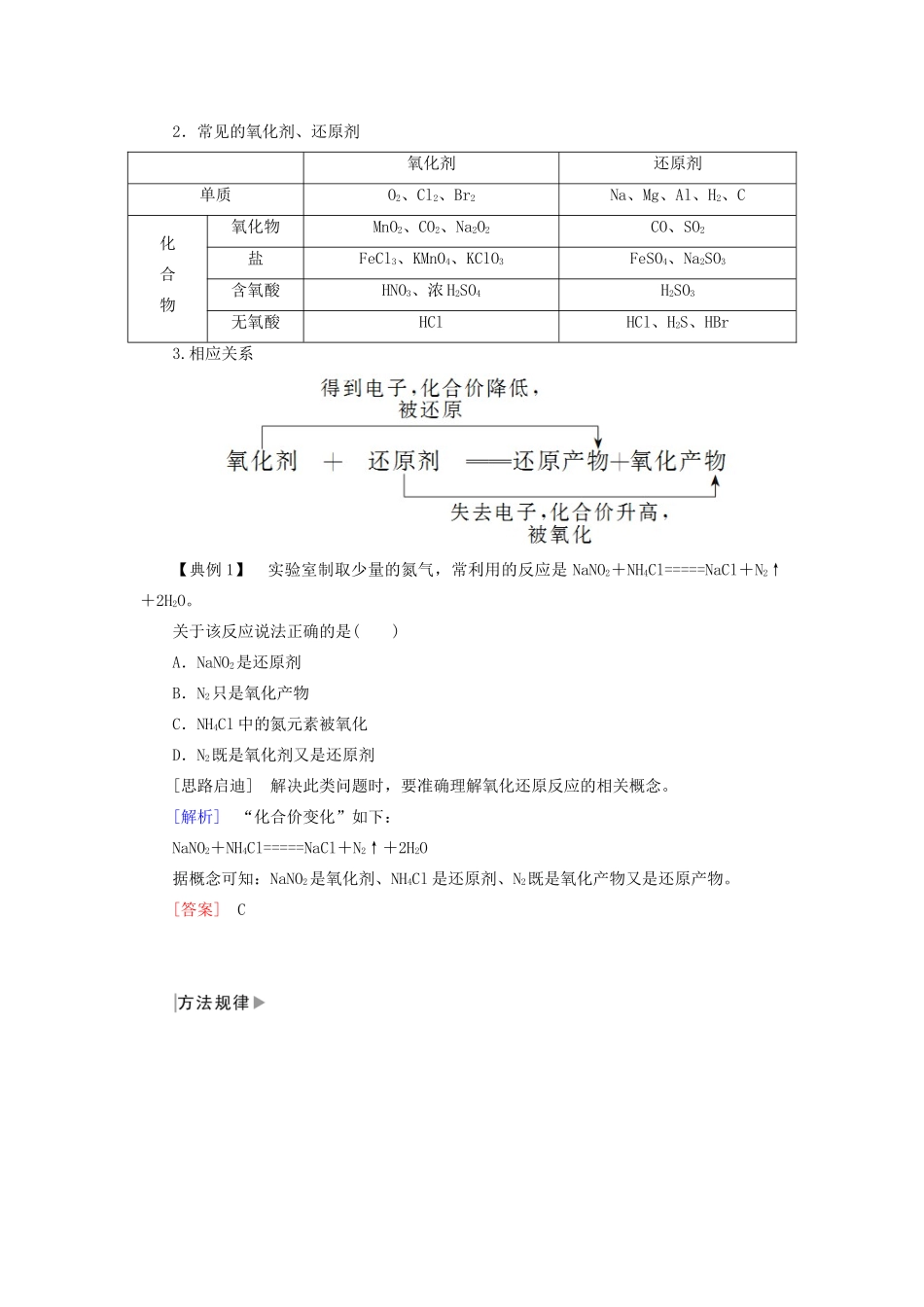
第二课时氧化剂和还原剂学习目标:1
认识氧化剂、还原剂、氧化性、还原性等基本概念
了解常见的氧化剂、还原剂
了解氧化还原反应的应用及基本规律
1.氧化剂和还原剂(1)氧化剂①氧化剂是得到电子(或电子对偏向)的物质,具有氧化性
②氧化剂在反应时所含元素的化合价降低,本身被还原
③常见的氧化剂:Cl2、O2等非金属单质,KMnO4、HNO3、H2O2等化合物
(2)还原剂①还原剂是失去电子(或电子对偏离)的物质,具有还原性
②还原剂在反应时所含元素的化合价升高,本身被氧化
③常见的还原剂:金属单质,C、H2等非金属单质,CO等化合物
2.氧化产物和还原产物(1)氧化产物:还原剂被氧化生成的物质
(2)还原产物:氧化剂被还原生成的物质
1.判断正误(正确的打“√”,错误的打“×”)(1)氧化剂得电子被氧化为还原产物()(2)非金属单质在反应中只作氧化剂()(3)在氧化还原反应中,金属单质作反应物时一定是还原剂()(4)还原剂失去电子具有氧化性()(5)元素处于最高化合价时一定具有强氧化性()[答案](1)×(2)×(3)√(4)×(5)×2.用“双线桥”表示下列反应的电子转移方向和数目,并在“反应物”“生成物”化学式下方注明氧化剂、还原剂、氧化产物、还原产物
(1)3CO+Fe2O3=====3CO2+2Fe______________________________________________________(2)2KClO3=====2KCl+3O2↑_______________________________________________________(3)2Na+Cl2=====2NaCl_______________________________________________________[答案]知识点一氧化剂、还原剂1
从电子转移角度认识氧化剂