第二节镁、铝及其重要化合物最新考纲:1
了解镁、铝及其重要化合物的制备方法
掌握镁、铝的主要性质及其应用
掌握镁、铝的重要化合物主要性质及其应用
核心素养:1
宏观辨识与微观探析:认识铝的化合物的两性,能从铝化合物的多样性,理解铝及其化合物的性质
科学探究与创新意识:能发现和提出有探究价值的有关铝及其化合物性质的探究方案,进行实验探究
知识点一镁及其化合物1.镁的物理性质(1)镁:镁是银白色有金属光泽的固体,密度较小,硬度较低、有延展性,是电和热的良导体
(2)镁合金:密度较小,硬度和强度都较大
2.镁及其重要化合物的性质3
镁的用途镁合金用于制造火箭、导弹和飞机的部件镁制造信号弹和焰火氧化镁熔点高,可作耐高温材料4
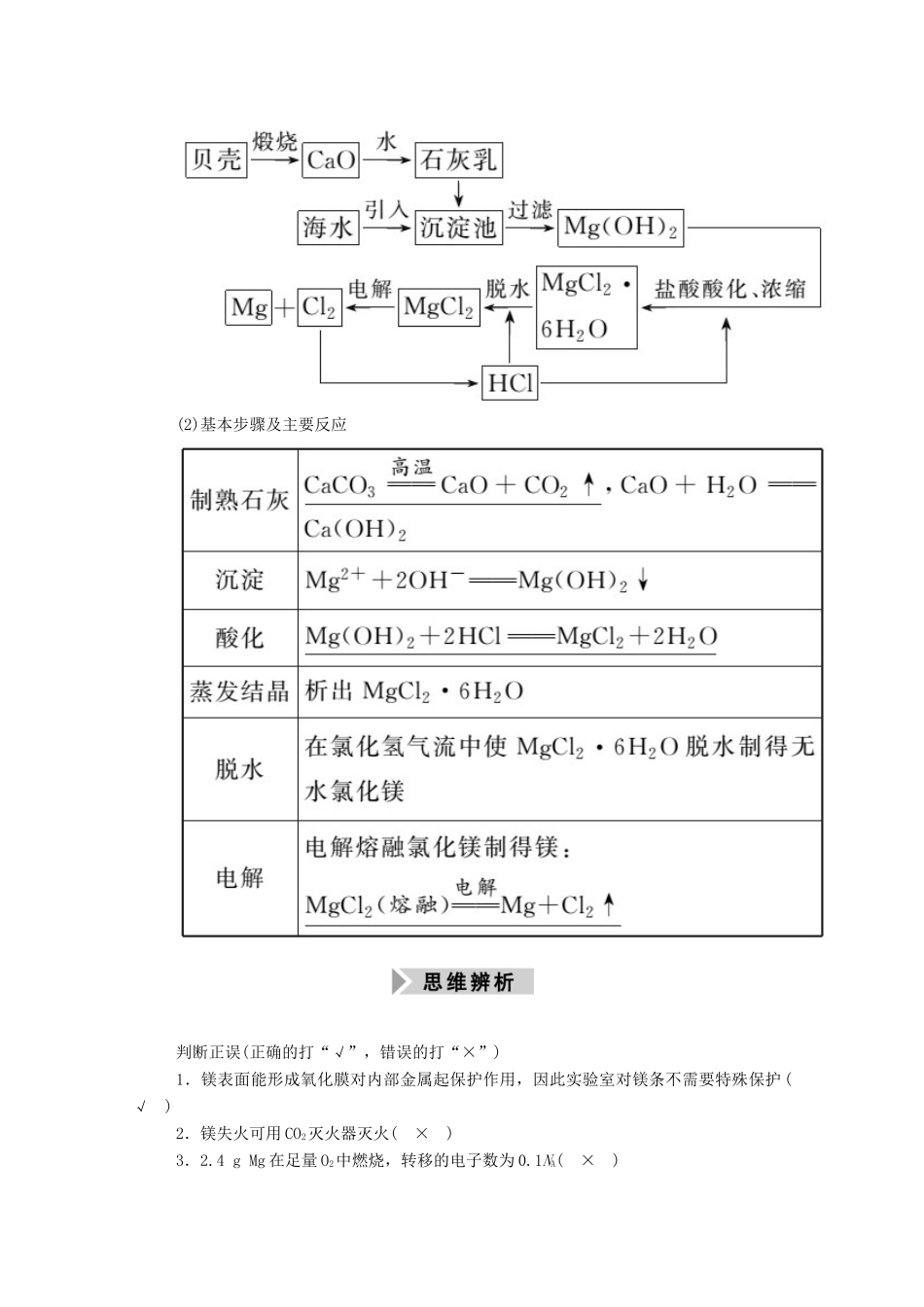
从海水中提取镁(1)工艺流程(2)基本步骤及主要反应判断正误(正确的打“√”,错误的打“×”)1.镁表面能形成氧化膜对内部金属起保护作用,因此实验室对镁条不需要特殊保护(√)2.镁失火可用CO2灭火器灭火(×)3.2
4gMg在足量O2中燃烧,转移的电子数为0
1NA(×)4.海水中提取镁所涉及的化学反应全部是氧化还原反应(×)5.将氯化镁晶体(MgCl2·6H2O)直接加热可制得无水氯化镁(×)6.有下列物质间转化:MgCO3――→MgCl2(aq)――→Mg(×)1.Mg在空气中燃烧得到的固体物质主要为MgO和少量Mg3N2及C的混合物
2.Mg着火后,不可用CO2灭火,应用沙土盖灭
3.Mg(OH)2为难溶于水的白色沉淀,故常用NaOH溶液检验Mg2+的存在
4.由于Mg(OH)2的溶解度比MgCO3的小,故水垢的主要成分中含有的是Mg(OH)2,而非MgCO3
5.由MgCl2·6H2O到无水MgCl2,必须在HCl气流中加热,以防MgCl2水解
6.因镁在高温下能与O2、N2、CO2等气体发生反应,故工业电解MgCl2得到的镁,应在H2氛