课时1物质的量的单位——摩尔发展目标体系构建1
结合宏观可称量的物质与难以称量的粒子之间的联系引入物质的量及其单位
培养学生“宏观辨识与微观探析”的核心素养
2.了解阿伏加德罗常数,摩尔质量的含义,培养学生“宏观辨识”的核心素养
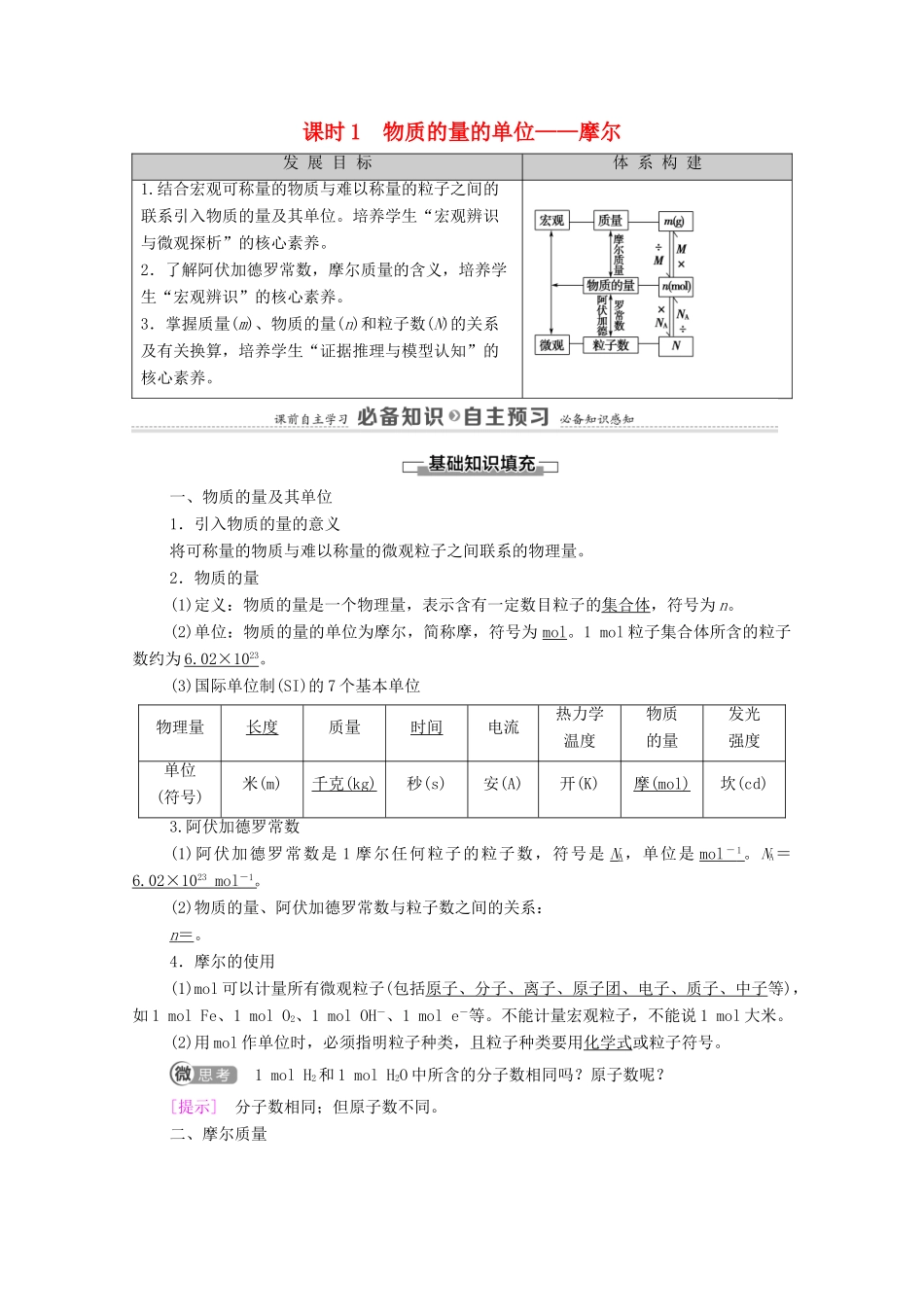
3.掌握质量(m)、物质的量(n)和粒子数(N)的关系及有关换算,培养学生“证据推理与模型认知”的核心素养
一、物质的量及其单位1.引入物质的量的意义将可称量的物质与难以称量的微观粒子之间联系的物理量
2.物质的量(1)定义:物质的量是一个物理量,表示含有一定数目粒子的集合体,符号为n
(2)单位:物质的量的单位为摩尔,简称摩,符号为mol
1mol粒子集合体所含的粒子数约为6
02×1023
(3)国际单位制(SI)的7个基本单位物理量长度质量时间电流热力学温度物质的量发光强度单位(符号)米(m)千克(kg)秒(s)安(A)开(K)摩(mol)坎(cd)3
阿伏加德罗常数(1)阿伏加德罗常数是1摩尔任何粒子的粒子数,符号是NA,单位是mol-1
02×1023mol-1
(2)物质的量、阿伏加德罗常数与粒子数之间的关系:n=
4.摩尔的使用(1)mol可以计量所有微观粒子(包括原子、分子、离子、原子团、电子、质子、中子等),如1molFe、1molO2、1molOH-、1mole-等
不能计量宏观粒子,不能说1mol大米
(2)用mol作单位时,必须指明粒子种类,且粒子种类要用化学式或粒子符号
1molH2和1molH2O中所含的分子数相同吗
[提示]分子数相同;但原子数不同
二、摩尔质量(1)一种微观粒子的摩尔质量就是1mol该微观粒子的质量,这种说法对吗
[提示]不对
摩尔质量的单位是g·mol-1,物质的质量单位是g,二者的意义不同
(2)已知1个氧原子的质量为2
657×10-26kg,请计算O2的摩尔质量为多