第一课时活泼的金属单质——钠学习目标:1
能记住金属钠的物理性质以及金属钠的用途
知道金属钠与氧气、水等反应的现象及化学方程式
1.钠的原子结构与性质的关系钠原子最外层只有1个电子,核外电子排布为,在化学反应中钠原子很容易失去1个电子形成最外层为8个电子的钠离子,核外电子排布为,达到稳定结构,因此金属钠的化学性质很活泼,在自然界中以化合态形式存在
2.钠的物理性质钠的物理性质既有金属的一般性,又有其特殊性:一般性:银白色金属,热和电的良导体
特殊性:质软,密度比水小,熔点低
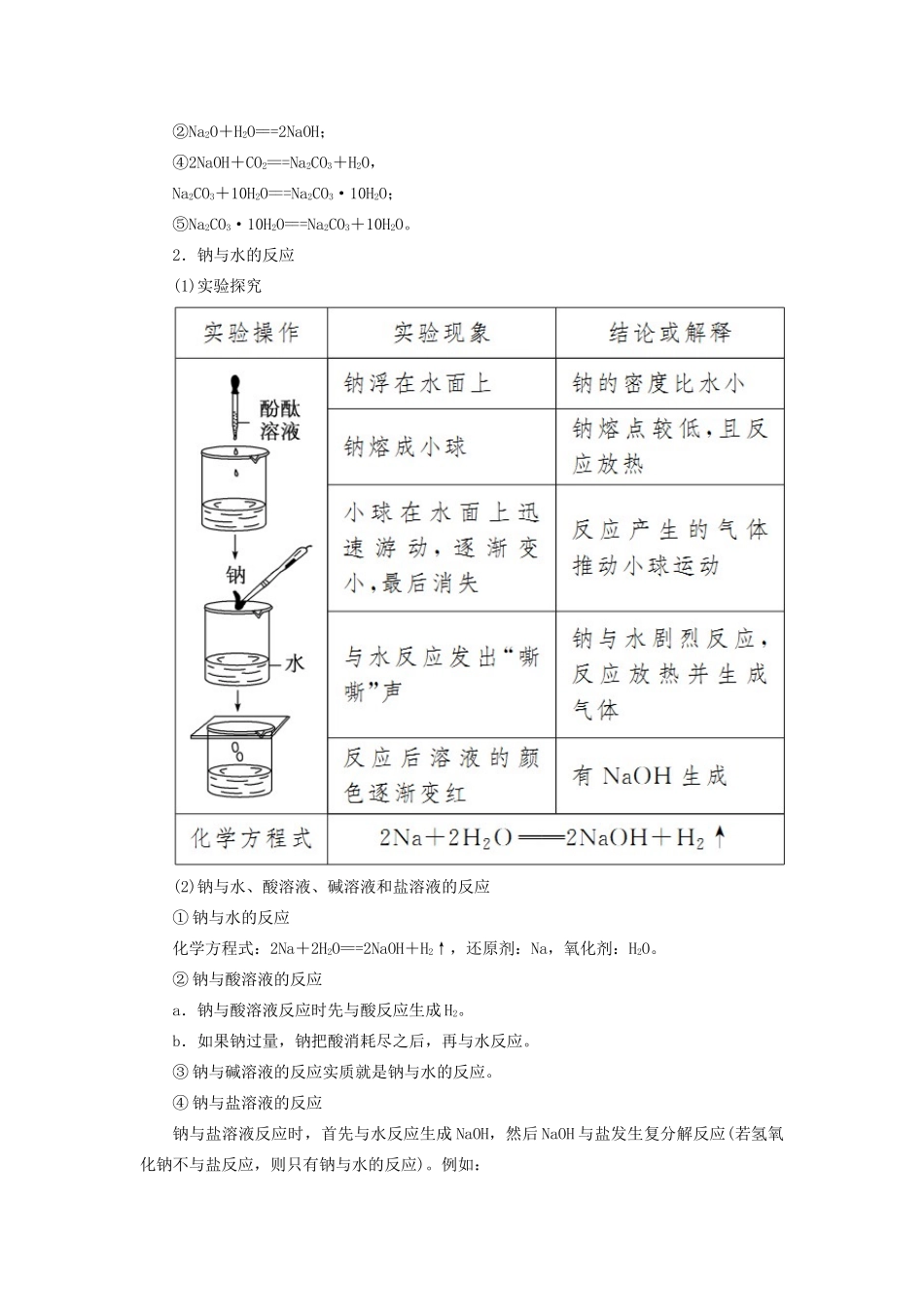
3.钠的化学性质写出下列反应的化学方程式:(1)钠在空气中表面变暗:4Na+O2===2Na2O;(2)钠在空气中燃烧:2Na+O2=====Na2O2;(3)钠与水反应:2Na+2H2O===2NaOH+H2↑
1.判断正误(正确的打“√”,错误的打“×”)(1)自然界中钠存在游离态()(2)钠的熔点低()(3)钠与O2反应时,条件不同,产物不同()(4)钠能与水发生置换反应()[答案](1)×(2)√(3)√(4)√2.取一块金属钠,放在燃烧匙里加热,下列对实验现象的描述正确的是()①金属先熔化②在空气中燃烧,产生黄色火花③燃烧后得白色固体④燃烧时火焰为黄色⑤燃烧后生成淡黄色固体A.②⑤B.①②③C.①④⑤D.④⑤[解析]钠燃烧时,先受热熔化成闪亮的小球,然后燃烧,燃烧时火焰为黄色,燃烧后生成淡黄色的过氧化钠固体
[答案]C知识点一钠1
钠与氧气的反应(1)实验探究(2)金属钠露置于空气中的主要变化金属钠长期露置于空气中最终完全转变为Na2CO3粉末,此过程中的主要变化与现象有:――→――→――→――→――→发生的主要变化的化学方程式为①4Na+O2===2Na2O;②Na2O+H2O===2NaOH;④2NaOH+CO2===Na2CO3+H2O,Na2CO3+10H2O===Na2CO3·1