第三章金属及其化合物第一节金属的化学性质第一课时金属与非金属的反应金属与酸和水的反应[学习目标]1
了解金属单质的物理性质和金属的通性
掌握钠、铝与氧气的反应,钠与水的反应及实验问题
掌握Fe与H2O(g)反应原理及其实验问题探究
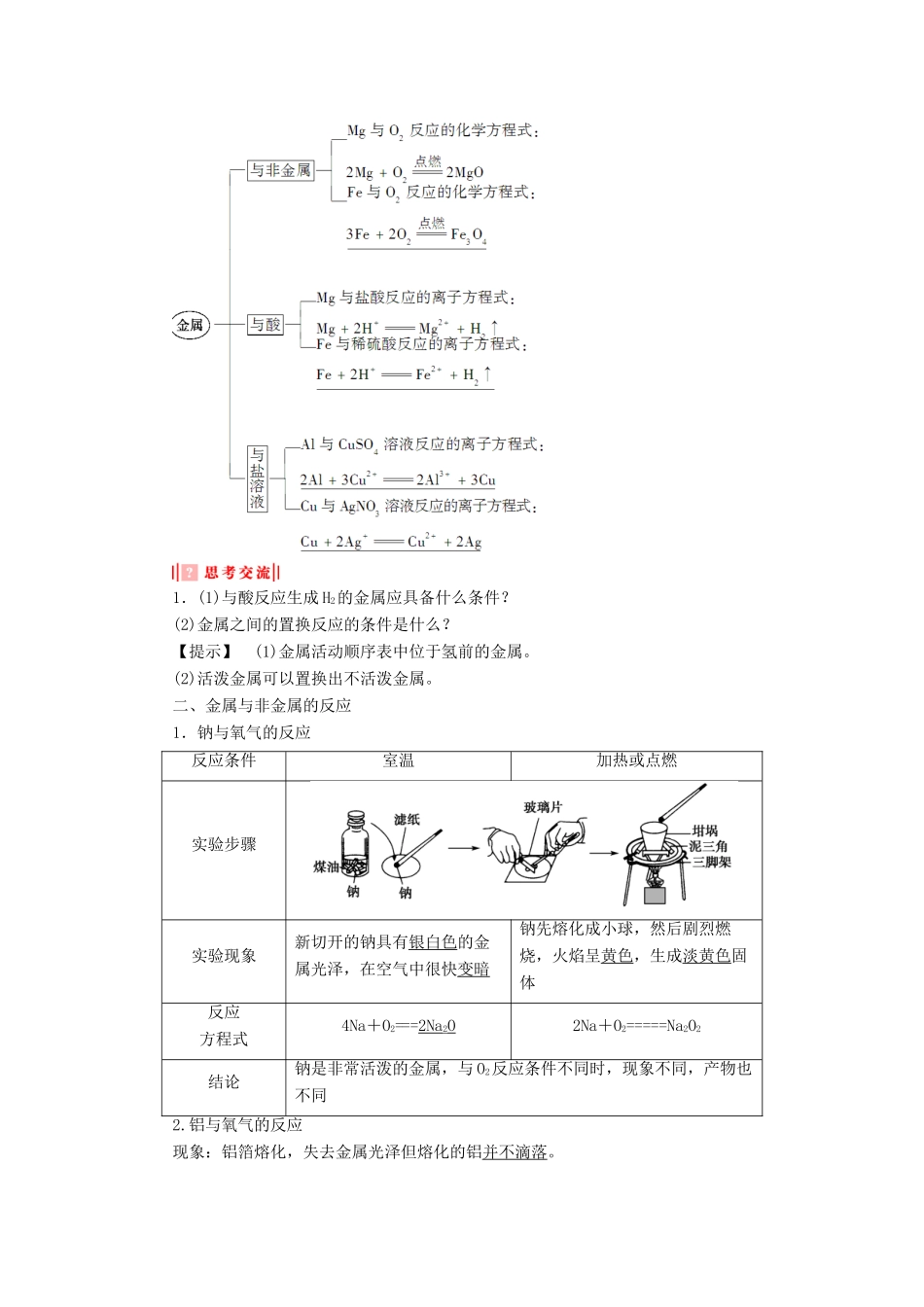
(重难点)一、金属的通性1.金属的物理性质2.化学性质1.(1)与酸反应生成H2的金属应具备什么条件
(2)金属之间的置换反应的条件是什么
【提示】(1)金属活动顺序表中位于氢前的金属
(2)活泼金属可以置换出不活泼金属
二、金属与非金属的反应1.钠与氧气的反应反应条件室温加热或点燃实验步骤实验现象新切开的钠具有银白色的金属光泽,在空气中很快变暗钠先熔化成小球,然后剧烈燃烧,火焰呈黄色,生成淡黄色固体反应方程式4Na+O2===2Na2O2Na+O2=====Na2O2结论钠是非常活泼的金属,与O2反应条件不同时,现象不同,产物也不同2
铝与氧气的反应现象:铝箔熔化,失去金属光泽但熔化的铝并不滴落
化学方程式:4Al+3O2=====2Al2O3
3.金属与Cl2、S的反应金属与Cl2、S等物质反应生成相应的氯化物、硫化物
如Na与Cl2反应化学方程式为:2Na+Cl2=====2NaCl
2.铝是活泼金属,为什么各种铝制品还能被较长时间使用和广泛应用
【提示】铝的性质非常活泼,常温下与O2反应生成致密的氧化膜,阻止了内层铝与氧气的继续反应
三、金属与酸、水的反应1.金属与酸的反应非氧化性酸(盐酸或稀硫酸)和金属活动性顺序表中氢以前的金属反应生成盐和氢气,如Zn、Fe和稀盐酸反应的离子方程式分别为Zn+2H+===Zn2++H2↑,Fe+2H+===Fe2++H2↑
2.金属与水的反应(1)钠与水的反应反应的化学方程式:2Na+2H2O===2NaOH+H2↑
(2)铁和水蒸气的反应方法一方法二实验装置操作及现象用小试管收集一试管