2元素周期律(第2课时)【学习目标】1、了解元素金属性、非金属性的周期性变化
2、了解元素周期表和元素周期律的意义
3、掌握元素周期表和元素周期律的应用
【重点难点】元素周期表和元素周期律的意义、元素周期律的应用【复习】1、元素原子核外电子排布规律有哪些
2、元素的主要化合价是如何随原子序数的递增而呈现周期性变化的
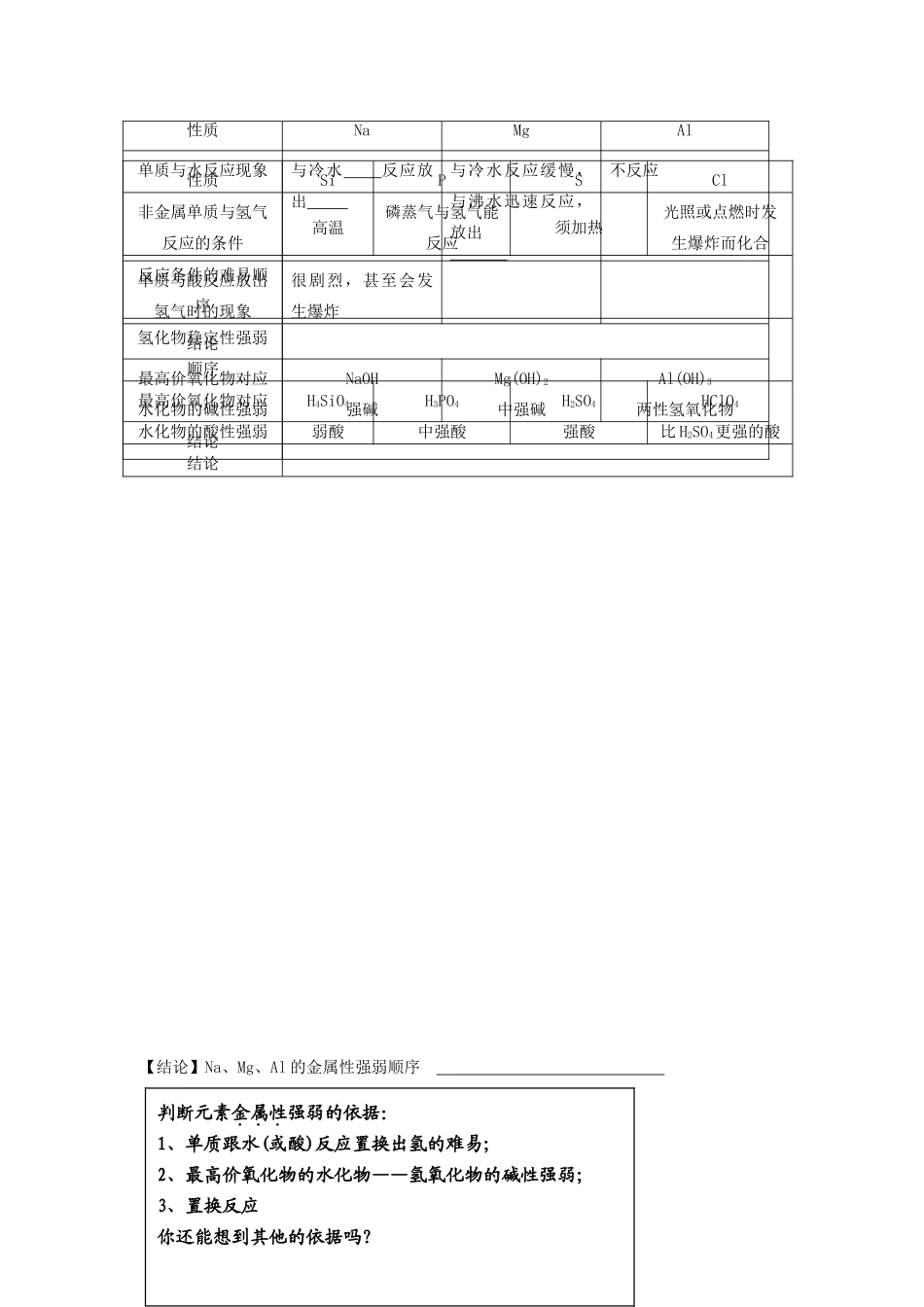
4、元素的金属性与非金属性变化规律『以11~18号元素为例』◆Na、Mg、Al三种金属元素的金属性强弱比较判断元素非金属性强弱的依据:1、跟氢气反应生成气态氢化物的难易程度以及氢化物的稳定性;2、元素最高价氧化物的水化物的酸性强弱
3、置换反应……【结论】Na、Mg、Al的金属性强弱顺序性质NaMgAl单质与水反应现象与冷水反应放出与冷水反应缓慢,与沸水迅速反应,放出不反应单质与酸反应放出氢气时的现象很剧烈,甚至会发生爆炸结论最高价氧化物对应水化物的碱性强弱NaOH强碱Mg(OH)2中强碱Al(OH)3两性氢氧化物结论性质SiPSCl非金属单质与氢气反应的条件高温磷蒸气与氢气能反应须加热光照或点燃时发生爆炸而化合反应条件的难易顺序氢化物稳定性强弱顺序最高价氧化物对应水化物的酸性强弱H4SiO4弱酸H3PO4中强酸H2SO4强酸HClO4比H2SO4更强的酸结论判断元素金属性强弱的依据:1、单质跟水(或酸)反应置换出氢的难易;2、最高价氧化物的水化物——氢氧化物的碱性强弱;3、置换反应你还能想到其他的依据吗
◆硅、磷、硫、氯四种非金属元素的非金属性强弱比较【结论】Si、P、S、Cl的非金属性强弱顺序【练习】(1)下述事实能够说明硫原子得电子能力比氯原子弱的是()A.硫酸比盐酸稳定B
氯化氢比硫化氢稳定C
盐酸酸性比氢硫酸强D
硫酸酸性比高氯酸弱(2)卤族元素的原子最外层上的电子数是,其中,非金属性最强的是
卤素的最高价氧化物对应水化物的化学式是(以X表示卤素)