课时2元素的性质与原子结构学习目标:1
了解碱金属元素和卤族元素在周期表中的位置及原子结构特征
了解碱金属元素、卤族元素性质的相似性和递变性
领悟同主族结构和性质的相似性和递变性
[自主预习·探新知]1.碱金属元素(1)碱金属元素的原子结构碱金属元素包括:Li、Na、K、Rb、Cs、Fr(写元素符号)
原子结构特点如下:①相似性:最外层电子数都是__1__
②递变性:Li―→Cs,核电荷数增大,电子层数增多,原子半径增大
(2)碱金属单质的物理性质(3)碱金属单质的化学性质性质或化学方程式相似性与O2①锂与氧气:4Li+O2=====2Li2O②钠与氧气:4Na+O2===2Na2O;2Na+O2=====Na2O2与H2O①钠与H2O:2Na+2H2O===2NaOH+H2↑②钾与H2O:2K+2H2O===2KOH+H2↑差异性与O2产物不同:Li-氧化物Li2O;Na-氧化物Na2O、过氧化物Na2O2;钾~铯生成更复杂的氧化物与H2O由锂到铯反应越来越剧烈2
卤族元素——简称卤素(1)卤族元素的原子结构卤族元素包括:F、Cl、Br、I、At(写元素符号)
原子结构特点如下:①相似性:最外层电子数都是____7____
②递变性:F→I,核电荷数增多,电子层数增多,原子半径增大
(2)卤素单质的物理性质F2Cl2Br2I2颜色、状态淡黄绿色气体黄绿色气体深红棕色液体紫黑色固体密度逐渐增大熔、沸点逐渐升高(3)卤素单质的化学性质①卤素单质与氢气的反应
从F2到I2(用“>”或“<”填写):反应的剧烈程度:F2>Cl2>Br2>I2;氢化物的稳定性:HF>HCl>HBr>HI
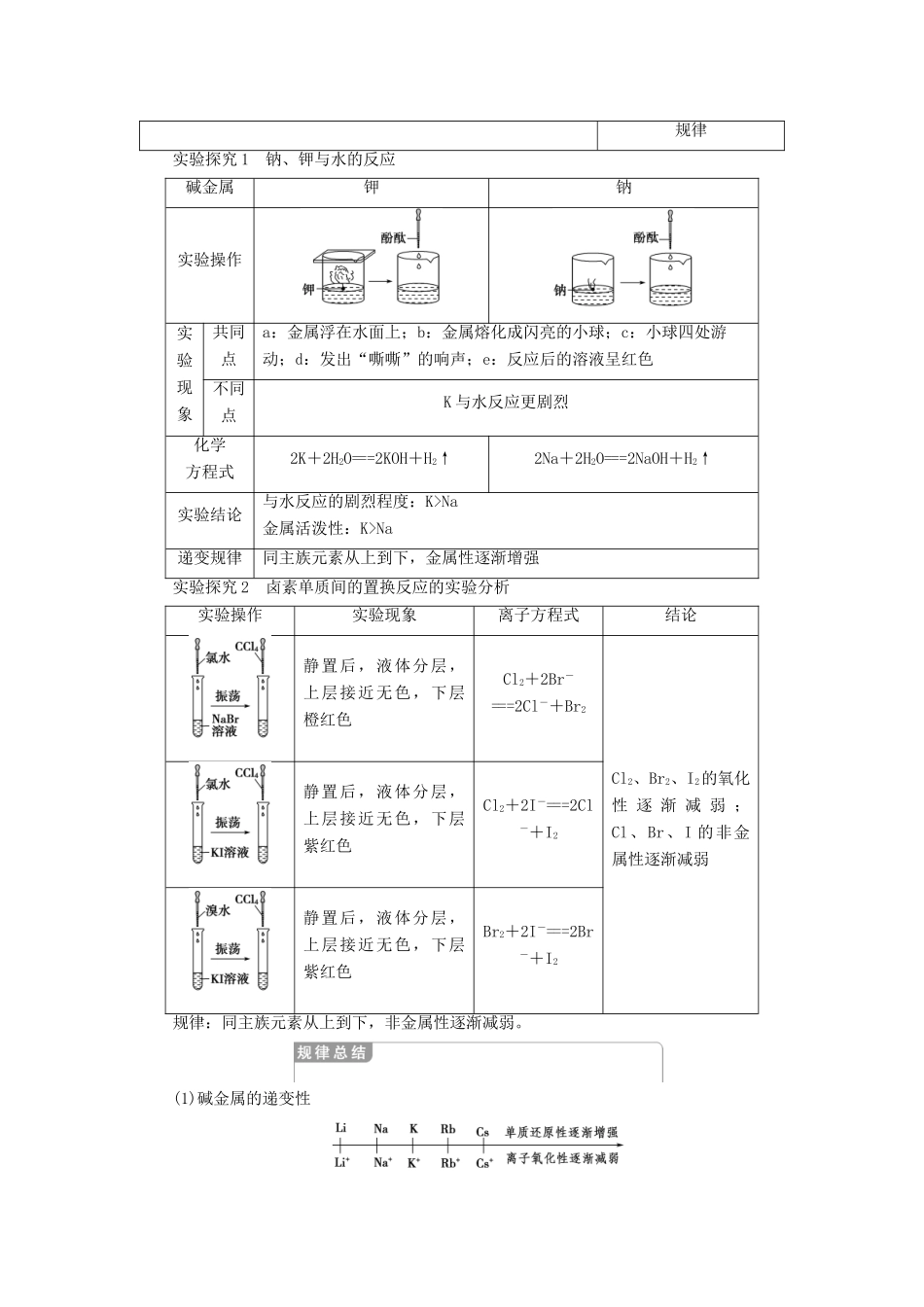
②卤素单质间置换反应(写出化学反应方程式)
将氯水加入NaBr溶液中:Cl2+2NaBr===2NaCl+Br2;将氯水加入KI溶液中:Cl2+2KI===2KCl+I2;将溴水加入KI溶液