共价键1.了解共价键、共价化合物的概念
2.了解化学键的概念
3.认识化学反应的实质
要点一1.Cl2的形成
(1)两个氯原子的最外层都有7个电子,要达到8电子稳定结构,都需获得1个电子,因此氯原子间难以发生电子得失,如果两个氯原子各提供1个电子,形成共用电子对,两个氯原子就都形成8电子稳定结构
(2)写出Cl2形成的过程
(3)结构式:在化学上,常用“—”表示一对电子,所得的式子叫结构式
Cl2的结构式Cl—Cl,H2的结构式H—H
(1)定义:原子间通过共用电子对所形成的相互作用
(2)成键粒子:原子
(3)成键元素:一般是同种或不同种非金属元素
①非金属元素的多原子单质,如H2、O2、O3、N2
②共价化合物,如HCl、H2O、CO2、H2SO4
③某些离子化合物,如NaOH、NH4Cl、Na2O2
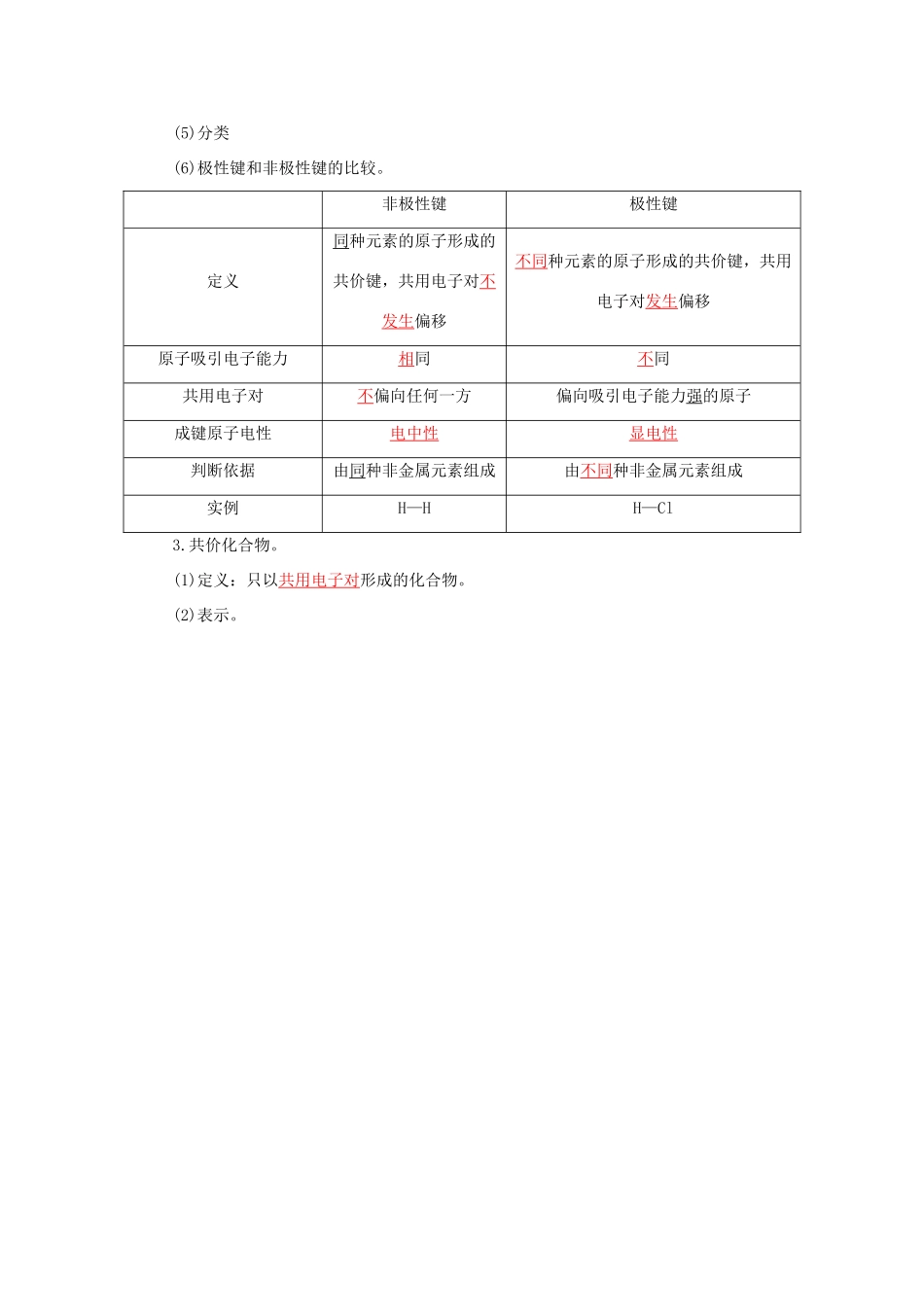
(5)分类(6)极性键和非极性键的比较
非极性键极性键定义同种元素的原子形成的共价键,共用电子对不发生偏移不同种元素的原子形成的共价键,共用电子对发生偏移原子吸引电子能力相同不同共用电子对不偏向任何一方偏向吸引电子能力强的原子成键原子电性电中性显电性判断依据由同种非金属元素组成由不同种非金属元素组成实例H—HH—Cl3
(1)定义:只以共用电子对形成的化合物
【应用思考】1.只有共价化合物中才含有共价键吗
共价化合物中一定含有共价键,单质和离子化合物中也可能含有共价键,如H2、O2、Cl2、NH4Cl、NaOH等均含有共价键
2.如何判断某共价键是极性键还是非极性键
提示:可根据成键元素的种类来判断
若成键元素相同,如X—X型,则为非极性键;若成键元素不同,如X—Y型,则为极性键
要点二1.定义:使离子相互结合或原子相互结合的作用力统称为化学键
3.化学反应的本质
物质发生化学反应的本质是旧化学键断裂与